1. AM:仿生纳米硅-胶原支架用于原位骨再生
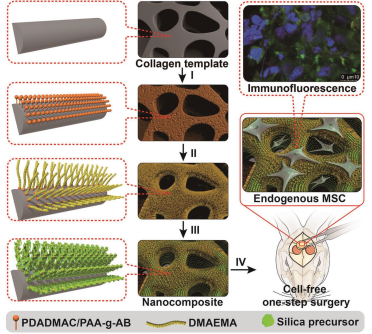
目前用于骨组织工程(BTE)的纳米硅-胶原(nSC)复合材料往往实现均匀的表面功能化,因此在“复制”天然骨的复杂结构和生物活性时能力有限。哈佛大学医学院Jinjun Shi教授、中科院化学研究所Xing Wang博士和北京大学第三医院余家阔教授合作利用一种生物硅化策略使多孔胶原支架具有均匀稳定的骨诱导表性面,因此合成的nSC复合材料具有天然骨样的多孔结构和纳米硅包覆层。
实验发现,nSC支架的骨诱导活性与硅包覆层的表面粗糙度和硅含量密切相关。在不使用外源性细胞和生长因子(GFs)的情况下,nSC支架可以对兔的颅骨缺损模型进行成功地修复,这是由于该nSC支架可协同激活与间充质干细胞募集和骨再生相关的多种信号通路。综上所述,这一研究所提出的表面生物硅化方法也可用于制备其他大尺寸、复杂的多孔结构和具有不同的骨诱导活性的BTE支架,具有很好的临床应用前景。
Shao-Jie Wang, Jinjun Shi, Xing Wang, Jia-Kuo Yu. et al. Biomimetic Nanosilica–Collagen Scaffolds for In Situ Bone Regeneration: Toward a Cell-Free, One-Step Surgery. Advanced Materials. 2019
DOI: 10.1002/adma.201904341
https://onlinelibrary.wiley.com/doi/10.1002/adma.201904341
2. ACS Nano:鞘内给药纳米簇用于保护神经元免受氧化应激作用
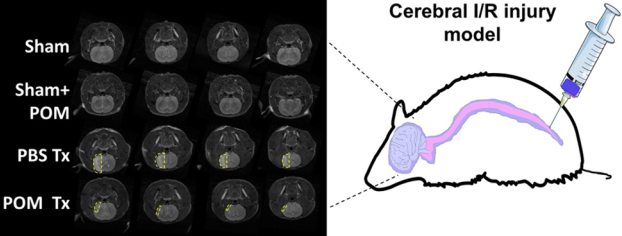
氧化应激是脑缺血再灌注(I/R)损伤的主要原因之一,而实现抗氧化剂在脑部的高效积累则有望有效防止大脑出现I/R损伤。威斯康星大学麦迪逊分校Dalong Ni博士和蔡伟波教授合作利用正电子发射断层成像(PET)技术,对纳米抗氧化剂多金属氧酸盐(POM)在大脑中的摄取进行了非侵入性地实时监测。
研究结果表明,POM纳米簇在被鞘内注射后会迅速到达缺血半暗区并有效清除活性氧(ROS),进而抑制氧化应激并使得脑I/R损伤模型的脑梗死面积显著缩小,神经功能恢复。这一研究表明,通过鞘内注射纳米抗氧化剂是改善脑I/R损伤的一种新型高效的治疗策略。
Shiyong Li, Dalong Ni, Weibo Cai. et al. Intrathecal Administration of Nanoclusters for Protecting Neurons against Oxidative Stress in Cerebral Ischemia/Reperfusion Injury. ACS Nano. 2019
DOI: 10.1021/acsnano.9b06780
https://pubs.acs.org/doi/10.1021/acsnano.9b06780
3. Nano Lett.:纳米RNP可以克服肿瘤治疗中的异质性问题
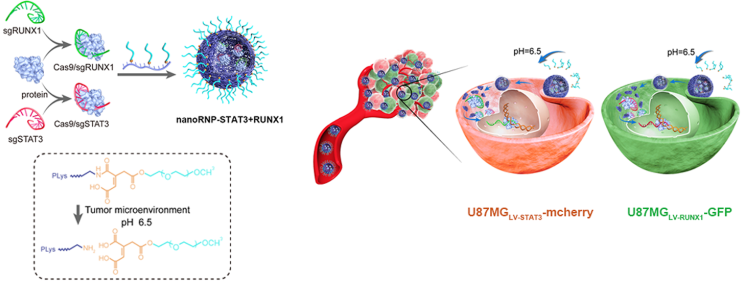
肿瘤的异质性是导致传统癌症治疗失败的重要因素之一,其出现的原因是在肿瘤发展过程中,肿瘤细胞亚群的遗传差异会不断地积累。由于肿瘤生长过程中遗传突变的多样性,联合使用多种药物对异种肿瘤进行治疗的效果也往往很有限。哈尔滨医科大学蒋传路教授、天津医科大学康春生教授、南开大学史林启教授和刘阳教授合作使用携带有sgRNAs、基于CRISPR/ cas9的纳米RNP来有效地解决肿瘤治疗中的异质性问题。
这种纳米RNP是由Cas9核糖核酸蛋白、sgRNAs以及响应性聚合物组合而成,它具有很好的体内循环稳定性、增强的肿瘤积累效果和在靶向的肿瘤细胞中进行高效基因编辑的能力。由于结合了可以靶向STAT3和RUNX1的sgRNAs,该纳米RNP可以在异质性肿瘤模型中高效地破坏基因表达并影响肿瘤细胞增殖,从而显著抑制异质性肿瘤的增长。
Qi Liu, Chuanlu Jiang, Linqi Shi, Chunsheng Kang, Yang Liu. et al. NanoRNP Overcomes Tumor Heterogeneity in Cancer Treatment. Nano Letters. 2019
DOI: 10.1021/acs.nanolett.9b02501
https://pubs.acs.org/doi/10.1021/acs.nanolett.9b02501
4. AFM:超声激活的纳米系统用于调节肿瘤微环境并增强声动力治疗
声动力治疗(SDT)是一种非侵入性、具有高穿透深度的治疗方法,在治疗深部实体肿瘤时具有很好的应用前景。然而,SDT的有效性往往也受到实体肿瘤乏氧微环境的限制。中科院上海硅酸盐研究所祝迎春研究员和上海交通大学郝永强教授合作,将高铁酸盐(VI)和原卟啉IX整合到可生物降解的中空介孔有机硅纳米材料中,然后将其和相变材料月桂酸进行组装开发了一种可被超声激活的纳米系统。
高铁酸盐(VI)与水以及肿瘤细胞中过表达的过氧化氢和谷胱甘肽(GSH)会发生反应,从而在肿瘤微环境中产生氧气并消耗GSH,活性氧(ROS)的产生则是通过原卟啉增强的SDT和细胞内发生的类芬顿反应来实现的。并且,超声诱导的温和热疗也可使得月桂酸发生相变,进而实现利用超声对氧和ROS的释放、GSH的消耗等过程的控制。研究结果表明,该纳米系统可以发挥生成氧气、原位消耗GSH和生成ROS等过程的协同作用来增强SDT对乏氧肿瘤的疗效,在体内外对骨肉瘤的生长都有显著的抑制效果。

Jingke Fu, Yingchun Zhu, Yongqiang Hao. et al. Ultrasound-Activated Oxygen and ROS Generation Nanosystem Systematically Modulates Tumor Microenvironment and Sensitizes Sonodynamic Therapy for Hypoxic Solid Tumors. Advanced Functional Materials. 2019
DOI: 10.1002/adfm.201906195
https://onlinelibrary.wiley.com/doi/10.1002/adfm.201906195
5. Small:功能化DNA对外泌体和囊泡进行编程进而用于肿瘤诊疗
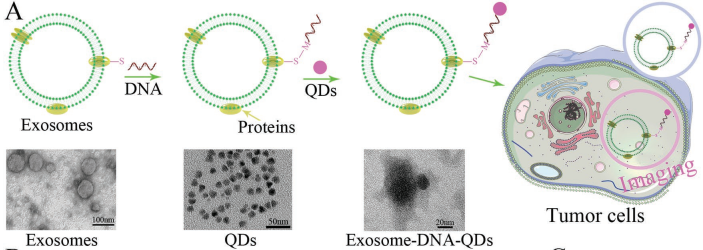
外泌体是一种调节许多生理和病理过程的重要信息载体。中山大学廖玉辉教授和黄曦教授合作,将功能化DNA作为铰链来将量子点(QDs)锚定在外泌体表面,进而设计了一种温和的生物标记策略。研究发现,被QDs标记的外泌体会迅速被肿瘤细胞吞噬,因此它可以作为一种标记肿瘤的特异性试剂。
此外,实验也通过气动脂质体挤出器构建了M1巨噬细胞(M1mv)的人工囊泡,结果发现M1mv可以有效杀死肿瘤细胞,实现理想的生物治疗效果。实验为了增强M1mv的抗肿瘤作用和药物释放的特异性,构建了靶向给药系统并实现了对特异性mRNA响应的药物递送和可视化肿瘤治疗。这一工作开发的策略大大促进了对外泌体和囊泡的标记以及功能化的效率,同时也构建了具有生物治疗和化疗功能的药物递送囊泡,从而为肿瘤的诊疗提供了新的思路。
Zhijin Fan, Yuhui Liao, Xi Huang. et al. Functionalized DNA Enables Programming Exosomes/Vesicles for Tumor Imaging and Therapy. Small. 2019
DOI: 10.1002/smll.201903761
https://onlinelibrary.wiley.com/doi/10.1002/smll.201903761
6. Nat. Rev. Cancer:脑瘤和脑转移瘤中存在的血脑屏障和血瘤屏障
治疗血源性癌症的试剂要发挥作用,必须穿过血管壁并克服癌细胞周围局部微环境的阻力才能到达更多的癌细胞中。而大脑的微环境则会严重阻碍药物对原发性脑肿瘤和脑转移瘤的治疗效果。已有研究表明,血脑屏障(BBB)的细胞和分子成分是一种用于维持大脑内环境稳定的神经血管单元。而肿瘤会破坏血脑屏障的完整性,从而产生一种被称为血瘤屏障(BTB)血管系统。
佐治亚理工学院Costas D. Arvanitis博士和哈佛大学医学院Rakesh K. Jain院士合作,对治疗脑瘤和脑部转移瘤时存在的血脑屏障和血瘤屏障进行了综述介绍;对血脑屏障及其对药物递送的影响、细胞类型对血脑屏障功能的影响以及血瘤屏障在疾病的发展和治疗中的作用进行了讨论;最后重点介绍了用于改善血脑屏障和药物递送的一些新型分子、细胞和生理学策略,并讨论了它们对改进免疫检查点抑制剂和工程化T细胞等传统和新兴治疗方法的作用。
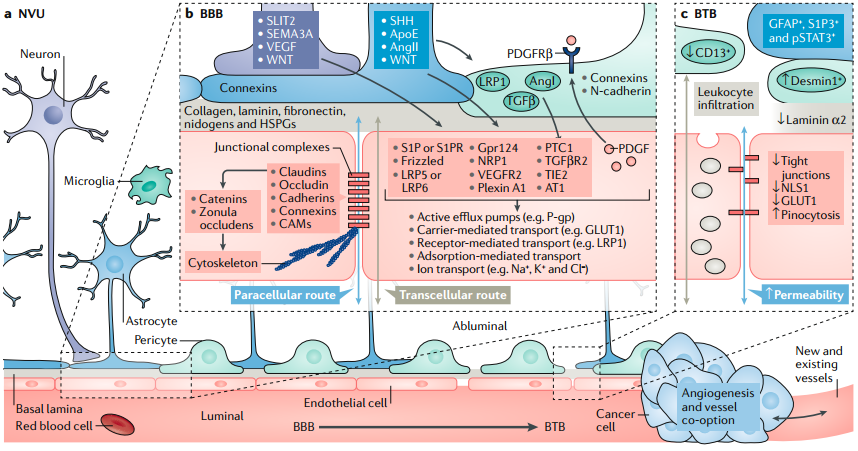
Costas D. Arvanitis, Rakesh K. Jain. et al. The blood–brain barrier and blood–tumour barrier in brain tumours and metastases. Nature Reviews Cancer. 2019
https://www.nature.com/articles/s41568-019-0205-x
7. Nature Mater.:弗林蛋白酶介导的奥沙拉嗪胞内自组装用于增强肿瘤诊疗
通过合理的设计使得探针或药物在和肿瘤特异性酶反应后不被泵出细胞,是目前增强造影剂或抗癌药物在肿瘤内的保留效果的策略之一。有鉴于此,约翰霍普金斯大学医学院Jeff W. M.Bulte团队将抗癌药物奥沙拉嗪 (Olsa)与细胞穿透肽RVRR相结合得到Olsa-RVRR,随后利用一种在生物学上很容易发生的缩合反应,使得单个Olsa-RVRR分子可以在与肿瘤相关的弗林蛋白酶的介导下在细胞内自组装成大的纳米颗粒。
由于Olsa具有可交换的羟基质子,因此Olsa-RVRR和Olsa纳米颗粒均可以实现化学交换饱和转移(CEST)磁共振成像(MRI)。实验使用HCT116和LoVo异种移植肿瘤小鼠模型进行体内研究,结果表明与没有RVRR的传统Olsa相比,结合有RVRR的Olsa在自组装后的CEST信号和抗肿瘤治疗效果分别增强了6.5倍和5.2倍,并且其成像信号和治疗响应(即归一化的肿瘤尺寸)之间也有着极好的线性相关 (R2 = 0.97)。综上所述,这一研究所开发的以弗林蛋白酶为靶点的磁共振成像平台具有对肿瘤的侵袭、药物的积累和治疗的响应进行有效评估的良好应用潜力。
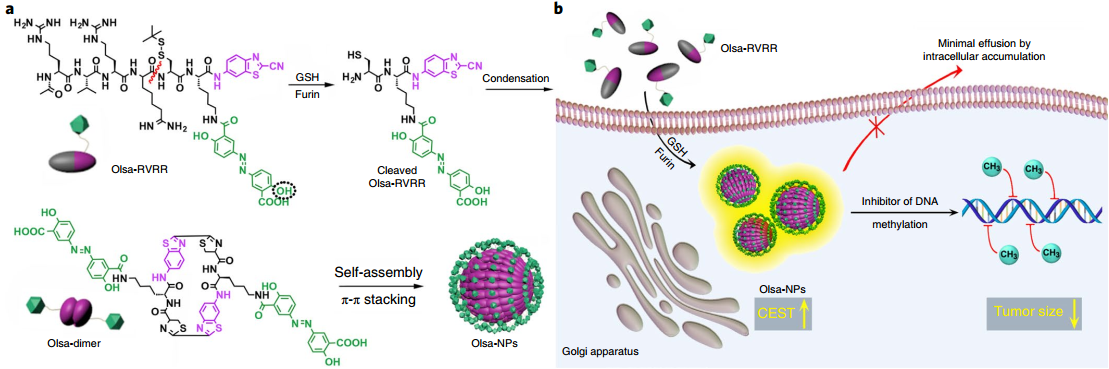
Yue Yuan, Jeff W. M. Bulte. et al. Furin-mediated intracellular self-assembly of olsalazine nanoparticles for enhanced magnetic resonance imaging and tumour therapy. Nature Materials. 2019
https://www.nature.com/articles/s41563-019-0503-4
8. Angew:可激活的NIR II纳米探针用于对外伤性脑损伤进行体内早期实时诊断
外伤性脑损伤(TBI)是一种具有高致残率和高致死率的急性疾病,并且目前的方法很难在早期对其进行有效诊断,也无法对其病理过程的进行有效的实时反馈。厦门大学李子婧博士和中科院苏州纳米所王强斌研究员合作制备了一种用于对TBI进行体内NIR II光学成像的靶向可激活荧光纳米探针(V&A@Ag2S)。由于从Ag2S和A1094发色团之间发生了能量转移,V&A@Ag2S的荧光在最开始是关闭的状态。
在被静脉注射后,V&A@Ag2S会通过血管细胞粘附分子1(VCAM1)介导的内吞作用在TBI炎症血管内皮迅速地积聚,随后通过TB I的前体生物标记物过氧亚硝酸盐(ONOO)对A1094进行漂白,使得Ag2S量子点(QDs)的NIR II荧光得以快速恢复。实验结果表明,该纳米探针通过利用NIR-II荧光成像的深组织穿透性和高信噪比以及对ONOO的高特异性、快速响应能力,为实现TBI的体内早期实时诊断提供了一种新的方法。
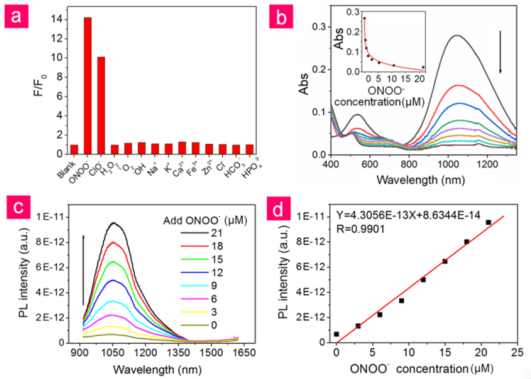
Chunyan Li, Wanfei Li, Zijing Li, Qiangbin Wang. et al. An Activatable NIR-II Nanoprobe for In Vivo Early Real-Time Diagnosis of Traumatic Brain Injury. Angewandte Chemie International Edition. 2019
DOI: 10.1002/anie.201911803
https://onlinelibrary.wiley.com/doi/10.1002/anie.201911803
9. Chem. Sci.:光致变色上转换纳米结构用于生物成像和双光控生成单线态氧
对单态氧(1O2)的生成进行精确控制是生物学和精准医学领域的研究热点。中科院国家纳米科学中心李乐乐研究员和赵宇亮院士合作,通过对包覆有介孔硅的上转换纳米颗粒(UCNP)进行控制合成构建了一种纳米结构,同时在其硅壁上共价嵌入了卟啉光敏剂(PSs),并将对NIR (808 nm)响应的二芳基乙基烯(DAE)光致变色开关负载到纳米孔中,因此它可以被双近红外光控制并产生1O2。
在980 nm NIR光照射下,内核的UCNP会吸收低能量的光子并将能量传递给硅壁上的PSs从而高效生成1O2。与此同时,当在纳米孔中的DAE处于闭环状态时,1O2的生成会被抑制,而当其受到808 NIR光照射后则会变成开环状态,从而使得该纳米结构生成1O2生成能力得以完全恢复。
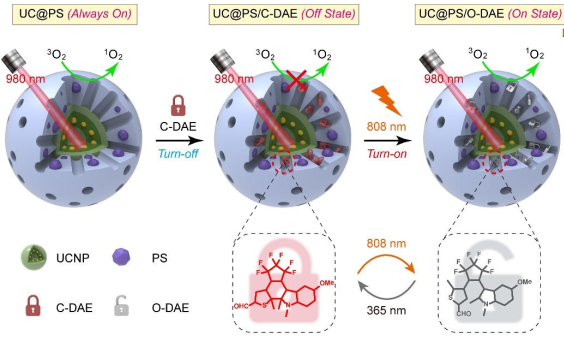
Yongsheng Mi, Yuliang Zhao, Lele Li. et al. Photochromic upconversion nanoarchitecture: towards activatable bioimaging and dual NIR light-programmed singlet oxygen generation. Chemical Science. 2019
DOI:10.1039/C9SC03524A
https://pubs.rsc.org/en/content/articlelanding/2019/sc/c9sc03524a#!divAbstract
10. AM:低剂量x射线激发凹面纳米立方体产生持久发光用于对肝脏肿瘤的成像
掺杂有铬的没食子酸锌ZnGa2O4:Cr3+ (ZGC)是一种能够持久发光(LLL)荧光材料,可以在体内成像检测中避免组织自身荧光干扰。ZGC在聚集态下是立方尖晶石结构,但纳米ZGC往往则是球形而非立方形,并且要在纳米尺度上使得ZGC保持良好的立方结构也是一个不小的难题。
国家同步辐射研究中心Hwo-Shuenn Sheu博士、高雄长庚纪念医院Chia-Hao Su博士和国立成功大学Chen-Sheng Yeh教授合作制备了具有良好分散性的凹面立方ZGC,与无法被低剂量(0.5 Gy)x射线激发的聚集态ZGC相比,立方ZGC在紫外和x射线激发下都表现出更强的LLL性能。并且该立方ZGC会在肝脏中发生特异性积累,并对原位肝肿瘤具有很好的被动靶向性,因此在被x射线激发结束后使用0.5 Gy的剂量就足以产生持久发光来对肝脏深部肿瘤进行成像。

Zheng-Zhe Chen, Chia-Hao Su, Hwo-Shuenn Sheu, Chen-Sheng Yeh. et al. Low Dose of X-Ray-Excited Long-Lasting Luminescent Concave Nanocubes in Highly Passive Targeting Deep-Seated Hepatic Tumors. Advanced Materials. 2019
DOI: 10.1002/adma.201905087
https://onlinelibrary.wiley.com/doi/10.1002/adma.201905087
11. ACS Nano:外渗的中性粒细胞会打开血管屏障并改善脂质体的药物递送效果
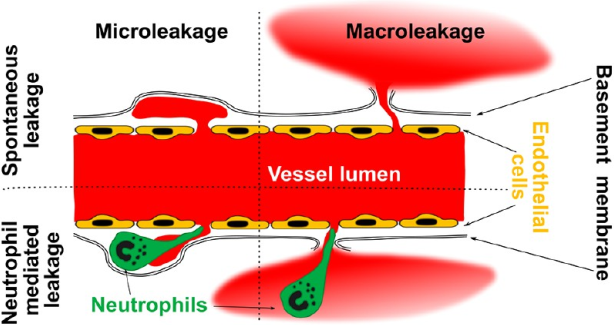
脂质体是在肿瘤治疗中应用最广泛的一种纳米载体。然而,尽管这些载体相对于游离的药物来说具有一定的优势,但其药物传递效率和靶向性仍有待进一步提高。俄罗斯国立科技大学Victor A. Naumenko团队使用活体荧光显微镜来对荧光脂质体在移植瘤模型(小鼠乳腺癌4T1、黑色素瘤B16和人类前列腺癌22Rv1模型)和正常皮肤中的行为进行研究并确定了两种主要的药物外渗模式:(1)微渗漏是一种在血管周围发生的局部纳米颗粒沉积的情况,它在恶性和健康组织中都会存在;(2)而宏渗漏则会深入组织并主要位于肿瘤-宿主界面。
虽然中性粒细胞没有摄取脂质体,但它们的外渗却会引发微渗漏和宏渗漏。研究结果发现,在接近中性粒细胞的地方往往更容易发现渗漏点,并且在研究的肿瘤类型中,中性粒细胞的数目也与渗漏的频率相关。这一研究表明,影响脂质体的外渗途径有望改善现有的治疗策略并为开发有效的肿瘤治疗纳米药物提供帮助。
Victor A. Naumenko, Kseniya Yu. Vlasova. et al. Extravasating Neutrophils Open Vascular Barrier and Improve Liposomes Delivery to Tumors. ACS Nano. 2019
DOI: 10.1021/acsnano.9b03848
https://pubs.acs.org/doi/10.1021/acsnano.9b03848
12. ACS Nano:NIR II光照激发材料生成的热和自由基用于增强肿瘤治疗
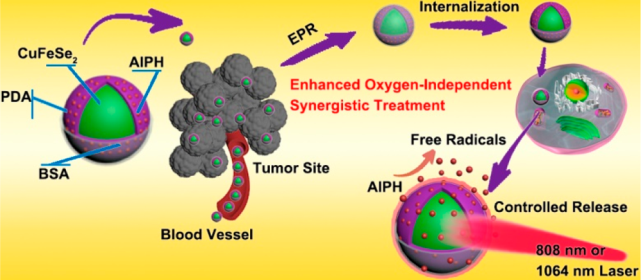
肿瘤细胞的代谢和肿瘤血管的增殖与正常细胞不同,由此产生的肿瘤微环境往往是乏氧的状态,这也极大限制了氧自由基的产生以及光动力治疗的疗效。中科院长春应化所林君研究员、哈尔滨工程大学冯莉莉博士和杨飘萍教授合作开发了一种不依赖氧的自由基生成纳米系统(CuFeSe2-AIPH@BSA),它在NIR I和NIR II区具有双峰吸收,因此可以用于进行成像指导的肿瘤协同治疗。
得益于这种特殊的吸收模式,该纳米系统在NIR I和NIR II区都有着很高的光热转换效率,因此其在近红外光照射下所产生的热量可使得AIPH释放并分解生成氧自由基,进而有效地杀死癌细胞。对比研究的结果表明,NIR II光相较于NIR I光来说有着更好的疗效,这主要是由于其具有更深的组织穿透和更高的安全剂量。体内研究表明,在肿瘤缺氧微环境中,利用NIR-II激光照射所产生的光热效应和毒性自由基可以很好地诱导癌细胞发生凋亡,进而抑制肿瘤的生长。
Jun Yang, Rui Xie, Piaoping Yang, Jun Lin. et al. Hyperthermia and Controllable Free Radical Coenhanced Synergistic Therapy in Hypoxia Enabled by Near-Infrared-II Light Irradiation. ACS Nano. 2019
DOI: 10.1021/acsnano.9b05985
https://pubs.acs.org/doi/10.1021/acsnano.9b05985
13. Nano Lett.:可聚集的纳米颗粒结合抗PD-L1抗体用于改善胶质瘤治疗
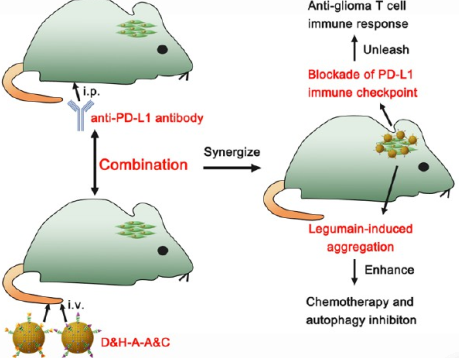
由于化疗药物在胶质瘤中的积累效率有限,且其自身存在多种生存机制如自噬和程序性细胞死亡配体1 (PD-L1)表达的上调等,因此通过靶向化疗对胶质瘤进行治疗的效果一直差强人意。四川大学高会乐教授团队提出了一种基于功能化金纳米颗粒(AuNPs)的、可以将化疗、自噬抑制和阻断PD-L1免疫检查点治疗相联合的治疗方案。实验设计了一种对豆荚蛋白响应的AuNPs (D&H-AA&C),它可以被动地靶向到胶质瘤部位,并在豆荚蛋白的作用下形成原位聚集物,进而增强DOX和HCQ在胶质瘤部位的积累。
HCQ可以抑制DOX诱导的细胞保护自噬,使胶质瘤细胞对DOX变得更加敏感。并且,抑制自噬也能抑制胶质瘤干细胞形成自噬相关的血管生成拟态(VM)。体内研究表明,D&H-A-A&C具有良好的抗胶质瘤作用,而通过和抗PD-L1抗体进行协同治疗后也能够逆转免疫抑制的肿瘤微环境,从而实现免疫响应,这样不仅可以进一步增强抗胶质瘤的效果,也能有效地预防肿瘤复发。综上所述,这一研究工作也为开发更有效、更个性化的胶质瘤联合治疗方案提供了新的思路。
Shaobo Ruan, Huile Gao. et al. Aggregable Nanoparticles-Enabled Chemotherapy and Autophagy Inhibition Combined with Anti-PD-L1 Antibody for Improved Glioma Treatment. Nano Letters. 2019
DOI: 10.1021/acs.nanolett.9b03968
https://pubs.acs.org/doi/10.1021/acs.nanolett.9b03968
14. AFM:Z型异质结功能化纳米片用于调节肿瘤微环境和增强肿瘤治疗作用
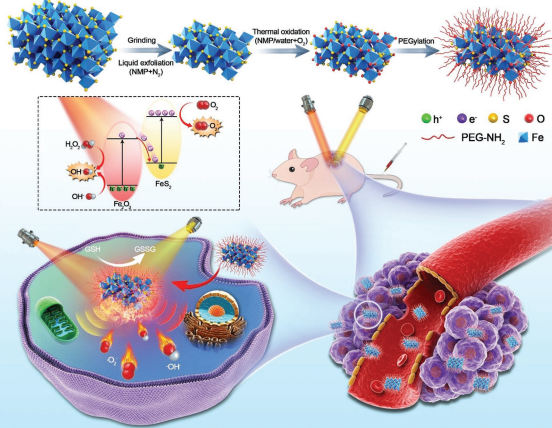
具有高电子-空穴分离效率和增强氧化还原电位的Z型异质结材料在光学诊疗领域有着很好的应用潜力。中山大学夏德华教授、梅林教授和姬晓元教授合作,在不同的溶液和空气环境下制备了新型的FeS2内核和Fe2O3外壳的二维纳米片(TOPY NSs)。TOPY NSs 的Fe2O3外壳和其内部的Fe3+/Fe2+均可通过消耗谷胱甘肽和产生O2来调节肿瘤微环境,并通过类芬顿反应产生·OH。
同时,FeS2内核和Fe2O3外壳也构成了一种Z型异质结,Fe2O3导带(CB)中的电子与FeS2价带(VB)中的空穴会发生重组,因而FeS2的CB和Fe2O3 的VB会具有更强的氧化还原电位。在650 nm激光照射下,O2和OH-会分别在FeS2的CB和Fe2O3的VB上生成·O2和·OH;而在808 nm激光照射下,NSs也可产生热量来用于进行光热治疗。并且该NSs也具有荧光、光声和光热成像等性能,因此是一种很好的多模态成像指导的癌症治疗平台。
Chao Pan, Dehua Xia, Lin Mei, Xiaoyuan Ji. et al. Z-Scheme Heterojunction Functionalized Pyrite Nanosheets for Modulating Tumor Microenvironment and Strengthening Photo/Chemodynamic Therapeutic Effects. Advanced Functional Materials. 2019
DOI: 10.1002/adfm.201906466
https://onlinelibrary.wiley.com/doi/10.1002/adfm.201906466
15. ACS Nano:聚合物脂质纳米颗粒利用淋巴结放大效应增强肠道和全身免疫反应
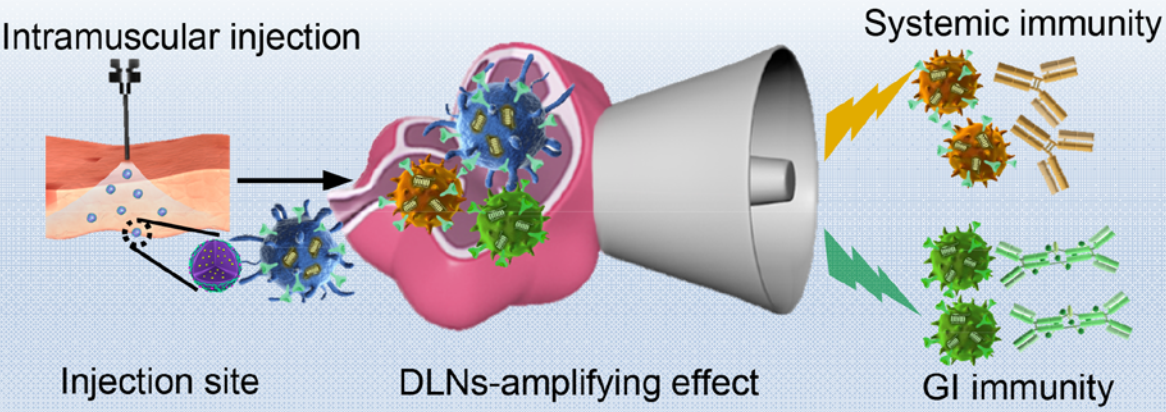
由于淋巴细胞会被局限于启动组织,因此肠外接种的疫苗无法同时激发产生有效的全身和胃肠道免疫保护效应。江南大学高晓东教授、中科院过程工程研究所吴颉研究员和马光辉研究员合作利用聚合物脂质纳米颗粒(PLNPs)去协同递送atRA、CpG和抗原,这样可以利用引流淋巴结(DLNs)的放大功能来实现肠道归巢并激活免疫。PLNPs在被肌肉注射后会在注射处形成一个免疫增强的环境,而其诱导启动的树突状细胞(DCs)会被指定转移到DLNs中。
DLNs的免疫增强环境可以显著增强免疫细胞间抗原的递呈和归巢受体的转换,同时刺激活化的淋巴细胞在周围组织和胃肠道组织内发生优先耗散。与目前含atRA的制剂相比,PLNPs不仅可以促进外周组织中IgG的分泌和T细胞的活化,而且在卵清蛋白和EV71疫苗接种实验中也能增强胃肠道中T细胞的归巢和抗原特异性IgA的水平。这一研究表明,利用DLN的放大效应可以刺激产生全身和胃肠道响应,从而进行更加有效的肠道疫苗接种。
Yiqun Du, Yufei Xia, Jie Wu, Xiao-Dong Gao, Guanghui Ma. et al. Exploiting the Lymph-Node-Amplifying Effect for Potent Systemic and Gastrointestinal Immune Responses via Polymer/Lipid Nanoparticles. ACS Nano. 2019
DOI: 10.1021/acsnano.9b04071
https://pubs.acs.org/doi/10.1021/acsnano.9b04071
16. Chem. Sci.:利用拉曼对光热治疗诱导细胞凋亡的分子信号通路进行观察
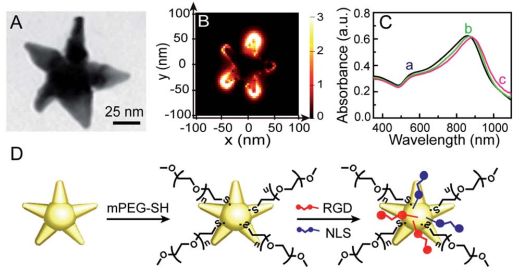
等离激元纳米颗粒(NP)介导的光热治疗(PPTT)是一种很好的微创癌症治疗方法,目前也已经发展到临床试验的早期阶段。而了解PPTT的细胞和分子响应对提高其治疗效果和临床应用进展至关重要。南京大学朱俊杰教授、南京师范大学吴萍教授和蔡称心教授合作,将核靶向的金纳米星(Au NSs)作为光热试剂去特异性诱导癌细胞发生凋亡;同时Au NSs也可作为表面增强拉曼光谱(SERS)的探针,对凋亡MCF-7细胞的时变SERS光谱进行监测。
实验利用这一策略,对PPTT诱导凋亡的分子信号通路进行了研究,包括细胞色素c的释放,蛋白质降解和DNA碎裂等。研究结果表明,PPTT诱导的细胞凋亡会经历一个线粒体介导的凋亡通路,而这一通路也被进一步证实是由仅含BH3区域的蛋白BID启动的。这一研究不仅有助于提高对PPTT诱导细胞凋亡的分子机制的基础认识,也有助于改善对PPTT的调控以进一步推动其临床应用。
Yingfang Xing, Ping Wu, Chenxin Cai, Jun-Jie Zhu. et al. Raman observation of a molecular signaling pathway of apoptotic cells induced by photothermal therapy. Chemical Science. 2019
DOI:10.1039/C9SC04389F
https://pubs.rsc.org/en/content/articlelanding/2019/sc/c9sc04389f#!divAbstract
17. Nano Lett.:生物矿化溶瘤病毒用于双模态成像指导的肿瘤治疗
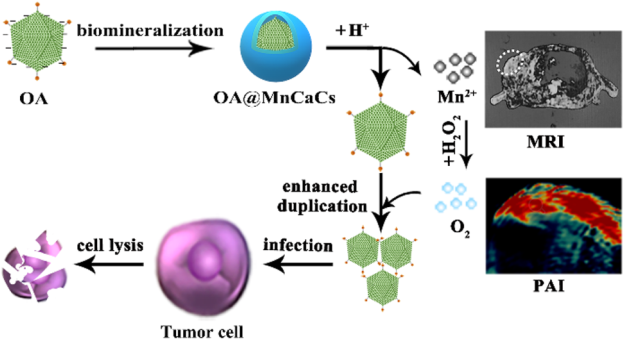
溶瘤腺病毒(OA)可以在肿瘤细胞中发生特异性复制,因此是一种很好的用于临床抗癌治疗的病毒。北京理工大学谢海燕教授团队创新性地利用钙锰碳酸盐 (MnCaCs)生物矿化层中对OA进行包裹,这样可以使得OA病毒不会被对宿主免疫系统清除,并延长其在体内的循环时间。
并且MnCaCs在肿瘤部位积累后会在酸性的微环境下溶解并释放出Mn2+,进而可将内源性的H2O2分解产生氧气(O2),从而增强OA的复制能力并显著提高其抗肿瘤疗效。同时,该材料也具有磁共振成像(MRI)和光声成像(PAI)的性能,可以在治疗过程中提供实时监测的信息。
Li-Li Huang, Hai-Yan Xie. et al. MnCaCs-Biomineralized Oncolytic Virus for Bimodal ImagingGuided and Synergistically Enhanced Anticancer Therapy. Nano Letters. 2019
DOI: 10.1021/acs.nanolett.9b03193
https://pubs.acs.org/doi/10.1021/acs.nanolett.9b03193
18. ACS Nano:NIR II分子靶向纳米探针用于免疫细胞的体内双色共聚焦成像
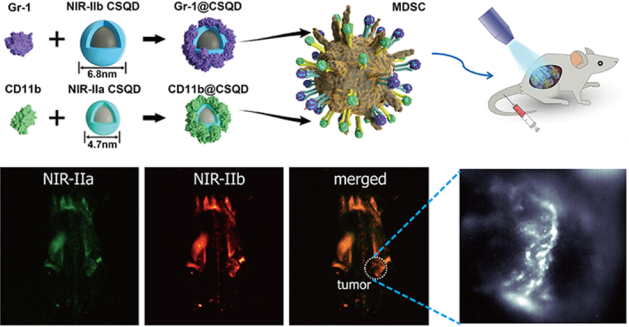
对体内的免疫细胞进行特异性监测可以有效地提高免疫治疗效果。武汉理工大学张明曦教授、武汉大学孙志军教授和崔然博士合作利用基于量子点(QD)的NIR II纳米探针来对免疫细胞(骨髓衍生抑制细胞(MDSC))进行体内双色荧光分子成像。
实验将NIR-IIa和NIR-IIb QDs分别与两种MDSC的特异性抗体进行结合,进而可以共靶向体内的MDSCs。由于NIR II光具有被抑制的光子散射和弱的自发荧光,因此通过该纳米探针进行双色荧光共聚焦成像可以对MDSCs在不同器官和组织中的分布进行研究。高分辨率成像实验结果则进一步对MDSCs在肿瘤免疫微环境中的确切分布进行了。这一研究的结果表明,具有分子靶向能力的NIR-II荧光纳米探针可以为实时监测体内免疫细胞群的动态变化提供有力的帮助,进而也为指导临床用药的选择和疗效评价提供了新的方法。
Guang-Tao Yu, Meng-Yao Luo, Zhi-Jun Sun, Ran Cui, Mingxi Zhang. et al. Molecular Targeting Nanoprobes with NonOverlap Emission in the Second Near-Infrared Window for in Vivo Two-Color Colocalization of Immune Cells. ACS Nano. 2019
DOI: 10.1021/acsnano.9b05038
https://pubs.acs.org/doi/10.1021/acsnano.9b05038
19. ACS Nano:共递送蜂毒肽和光敏剂的纳米载体用于光动力-免疫联合治疗
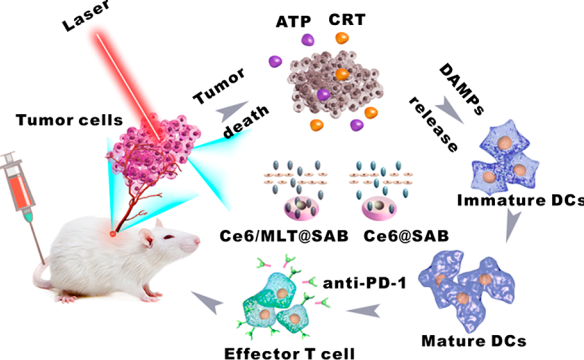
光动力治疗(PDT)是一种通过诱导产生活性氧(ROS)来治疗癌症的方式,并且ROS也会引发免疫原性细胞死亡(ICD)。为了同时提高PDT介导的细胞内ROS生成和ICD水平,湖北大学徐祖顺教授、华中科技大学金红林博士和杨坤禹教授合作设计了一种血清白蛋白(SA)包裹的勃姆石(B)纳米载体,并利用其负载光敏剂Ce6 (Ce6)和蜂毒肽(MLT)。Ce6/MLT@SAB的粒径约为180 nm,相对于游离的MLT来说,Ce6/MLT@SAB可显著降低溶血现象,同时也能在体外实现MLT增强的PDT抗肿瘤效果。
与Ce6@SAB相比,Ce6/ MLT@SAB可以改善Ce6对癌细胞的穿透,从而在660 nm光照下增强细胞内ROS的生成。并且经光照后,被Ce6/MLT@SAB处理的细胞的ICD水平会有显著提高,同时也能有效激活树突状细胞。体内研究表明,在没有激光照射的情况下,与对照组相比,多次注射Ce6/MLT@SAB可使皮下小鼠肿瘤的生长被有效地抑制。当联合激光照射后,单次注射Ce6/MLT@SAB即可根除三分之一的小鼠皮下肿瘤。而若进一步联合免疫检查点阻断剂则能更好地增强其抗肿瘤作用,提高在肿瘤中产生的CD4+和CD8+ T细胞数量,同时减少骨髓衍生抑制细胞。
Haojie Liu, Yan Hu, Zushun Xu, Honglin Jin, Kunyu Yang. et al. Co-delivery of Bee Venom Melittin and a Photosensitizer with an Organic−Inorganic
Hybrid Nanocarrier for Photodynamic Therapy and Immunotherapy. ACS Nano. 2019
DOI: 10.1021/acsnano.9b04181
https://pubs.acs.org/doi/10.1021/acsnano.9b04181
20. Angew:MOF介导的光动力治疗和CpG递送以增强抗原递呈和癌症免疫治疗
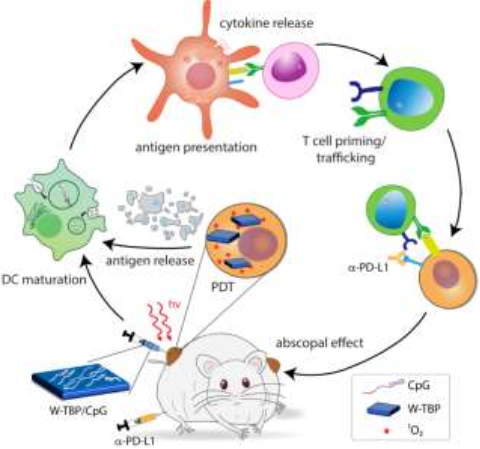
检查点阻断免疫治疗(CBI)可以唤醒宿主固有的免疫系统,通过重新激活细胞毒性T细胞来引起癌症患者的持续性响应。芝加哥大学林文斌教授团队制备了一种阳离子纳米MOF材料W-TBP,它可以通过进行免疫原性光动力治疗(PDT)和促进树突状细胞(DCs)的成熟来促进肿瘤抗原的表达。由双核的WVI二级构建单元和光敏剂卟啉(TBP)配体组成的阳离子W-TBP可以通过介导PDT来释放肿瘤相关抗原,并向DCs递送免疫刺激的CpG寡脱氧核苷酸。
研究结果表明,通过增强抗原呈递与CBI的协同作用可以使细胞毒性T细胞恢复活力并扩散,从而在双侧乳腺癌模型中实现极好的抗癌效果,可以有效地治愈(>97%)肿瘤。
Kaiyuan Ni, Wenbin Lin. et al. Nanoscale Metal-organic Frameworks Mediate Photodynamic Therapy and Deliver CpG Oligodeoxynucleotides to Enhance Antigen Presentation and Cancer Immunotherapy. Angewandte Chemie International Edition. 2019
DOI: 10.1002/anie.201911429
https://onlinelibrary.wiley.com/doi/10.1002/anie.201911429
21. Adv. Sci.综述:胞外囊泡在肿瘤免疫微环境和肿瘤免疫治疗中的作用
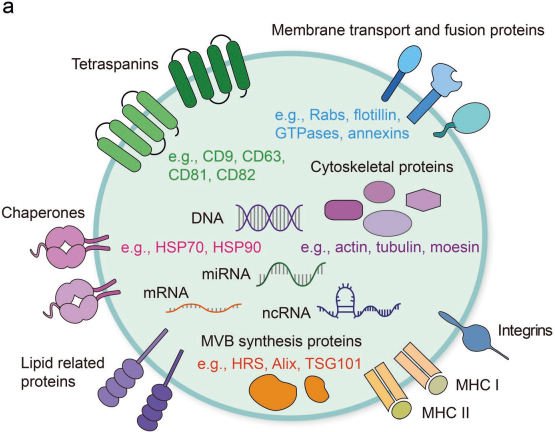
几乎所有的细胞都可以分泌胞外囊泡(EVs)。EVs可以将母体细胞的蛋白质、脂质和核酸递送给受体细胞,因此EVs也起着细胞间通讯和分子转移的中介作用。外泌体是EVs的一个小亚群,它会参与多种生理和病理过程,并且在肿瘤发生和转移前就会参与肿瘤免疫微环境的重建。同时,来自肿瘤细胞和宿主细胞的外泌体也会介导参与它们的相互作用过程,从而影响癌症治疗的响应性。而源于肿瘤的循环外泌体也被认为是早期诊断肿瘤的一种非侵入性的生物标志物。
基于外泌体的肿瘤治疗也正逐渐发展成为一种很有前途的新型策略,可用于抑制肿瘤发展或者增强抗肿瘤免疫。苏州大学周芳芳教授团队综述了外泌体及其在调节免疫响应中的关键作用和的治疗应用;同时也指出了当前研究的一些局限性并对未来的研究方向进行了展望。
Feng Xie, Fangfang Zhou. et al. Extracellular Vesicles in Cancer Immune Microenvironment and Cancer Immunotherapy. Advanced Science. 2019
DOI: 10.1002/advs.201901779
https://onlinelibrary.wiley.com/doi/full/10.1002/advs.201901779
22. AFM:将细菌-光热治疗和抗PD -1肽结合以增强晚期癌症的免疫治疗
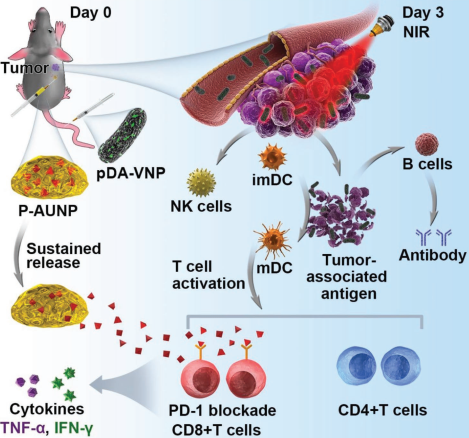
光热治疗(PTT)是一种很有前途的癌症治疗方法,但迄今为止它只能在相对较小的皮下肿瘤模型上才能成功,而治疗较大的肿瘤(200 mm3)则较为困难,这是因为大多数的PTT试剂都无法有效地到达肿瘤中心。并且免疫抑制的肿瘤微环境也会阻止T细胞去对抗残余的肿瘤细胞,从而导致肿瘤的复发和转移。四川大学孙逊教授团队将广泛使用的PTT材料聚多巴胺包覆在兼性厌氧菌VNP20009的表面,使其可以深入到更大的肿瘤中。
实验将包被的细菌进行静脉注射并随后在肿瘤部位进行近红外激光照射,同时局部接种含有抗程序化细胞死亡-1(PD -1)肽AUNP-12的磷脂相分离凝胶。该凝胶可以持续释放AUNP-12(42天)以逆转免疫抑制的肿瘤微环境。实验使用小鼠黑素瘤模型证明了这种将生物疗法、PTT和可持续的PD-1封锁相结合的联合治疗可以在80天内对50%的动物产生强大的抗肿瘤免疫响应并有效治愈相对较大的肿瘤。
Wenfei Chen, Xun Sun. et al. Combination of Bacterial-Photothermal Therapy with an Anti-PD-1 Peptide Depot for Enhanced Immunity against
Advanced Cancer. Advanced Functional Materials. 2019
DOI: 10.1002/adfm.201906623











