
第一作者:李世美
通讯作者:孟宪伟、谭龙飞
第一单位:中国科学院理化技术研究所
核心内容:
1. 综述了纳米金属有机框架(NMOFs)的合成方法,研究讨论了其生物相容性及荧光、MR、CT成像性能。
2. 系统讨论了NMOFs在肿瘤治疗中的应用,包括光疗、放疗、微波疗法及声动力治疗。
纳米金属有机框架
纳米金属有机框架(NMOFs)具有生物相容性好、比表面积大、结构可调、功能多样等优点,在生物医学应用领域越来越受到高度重视。
综述简介
有鉴于此,中国科学院理化技术研究所孟宪伟课题组系统介绍了纳米金属有机框架在肿瘤治疗相关研究中的最新进展。概括了NMOFs的合成方法、生物相容性及成像性能;系统分析并总结了NMOFs在包括光疗、放疗、微波疗法及声动力治疗在内的肿瘤治疗中的应用,并对其发展前景和挑战进行总结。
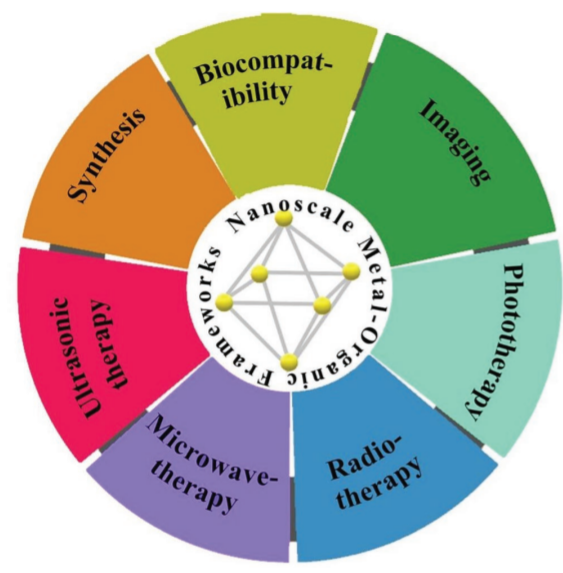
图1. 纳米金属有机框架应用。
要点1:NMOFs的合成、生物相容性及成像
1. 合成
MOFs由金属中心和有机配体组装而成,不同的金属离子和配体、反应溶剂、时间及温度都使得MOFs获得个性化特征。金属离子与配体之间的亲和力影响纳米结构的成核、形成及最终形态;在成核过程中,体系的温度和反应物的溶解度对反应位点的产生有重要影响,通常,较好的溶解度会促使体系产生更多的位点及更小的纳米尺度基元,从而促进大量小纳米颗粒的形成。文章综述了包括溶剂热法、微波辅助法、超声合成法和电化学法在内的四种合成方法,并分别就各影响因素进行讨论。
2. 生物相容性
NMOFs中金属离子与有机配体的可选择性、及其固有的可降解性为其良好的生物相容性奠定了基础。材料的生物相容性与其理化性质密切相关,在选择生物安全性高的金属离子及有机配体的前提下,综述了NMOFs的尺寸、表面性质及形貌对其在生物体内的运转、分布、内吞及代谢等方面的重大影响。同时,概述了影响尺寸及表面性质的因素,以及对二者进行调控和优化的方法,以确保合成生物相容性高的NMOFs来应用于肿瘤的诊断与治疗。
3. 成像
体内成像为实时检测和跟踪病变的发生、发展提供了一个可视化系统,在癌症的诊断与治疗中至关重要。NMOFs作为一种金属离子与有机配体可调、表面活性位点丰富的周期性多孔纳米材料,在生物成像中显现了重大的优势。通过选择功能性的金属离子或配体、通过化学配位或多孔性负载成像试剂,赋予了NMOFs荧光、MR及CT成像的功能。
要点2:NMOFs在肿瘤治疗中的应用
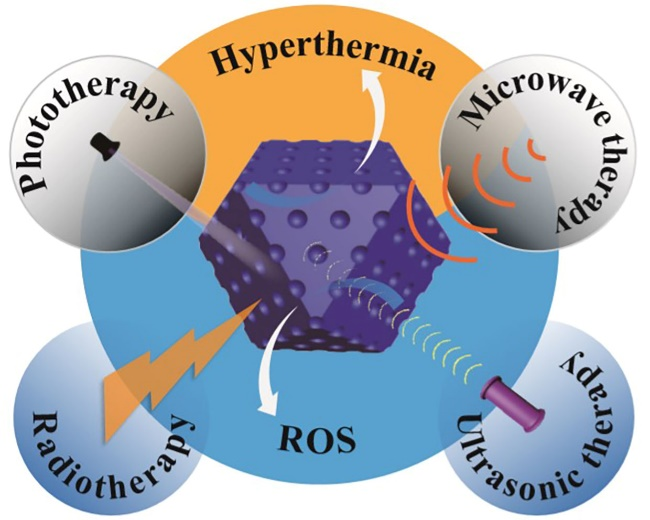
图2. NMOFs在四种肿瘤治疗中产热或产活性氧的示意图。
1. 光疗
光疗包括光动力及光热治疗。光动力疗法中,卟啉及其衍生物作为光敏剂与金属离子配位形成卟啉基NMOFs,NMOFs的周期性多孔结构有效地避免了光敏剂的自聚集和自猝灭,并提高了细胞毒性ROS的扩散效率。同时,良好的生物相容性及EPR被动靶向特性也使得NMOFs在光动力疗法中凸显出优势;光热疗法中,利用MOFs的多孔结构可将多种光热试剂负载于孔内。此外,还可通过将光热试剂(如IR825、ICG等)作为配体,实现NMOFs基光热系统的有效光热治疗。
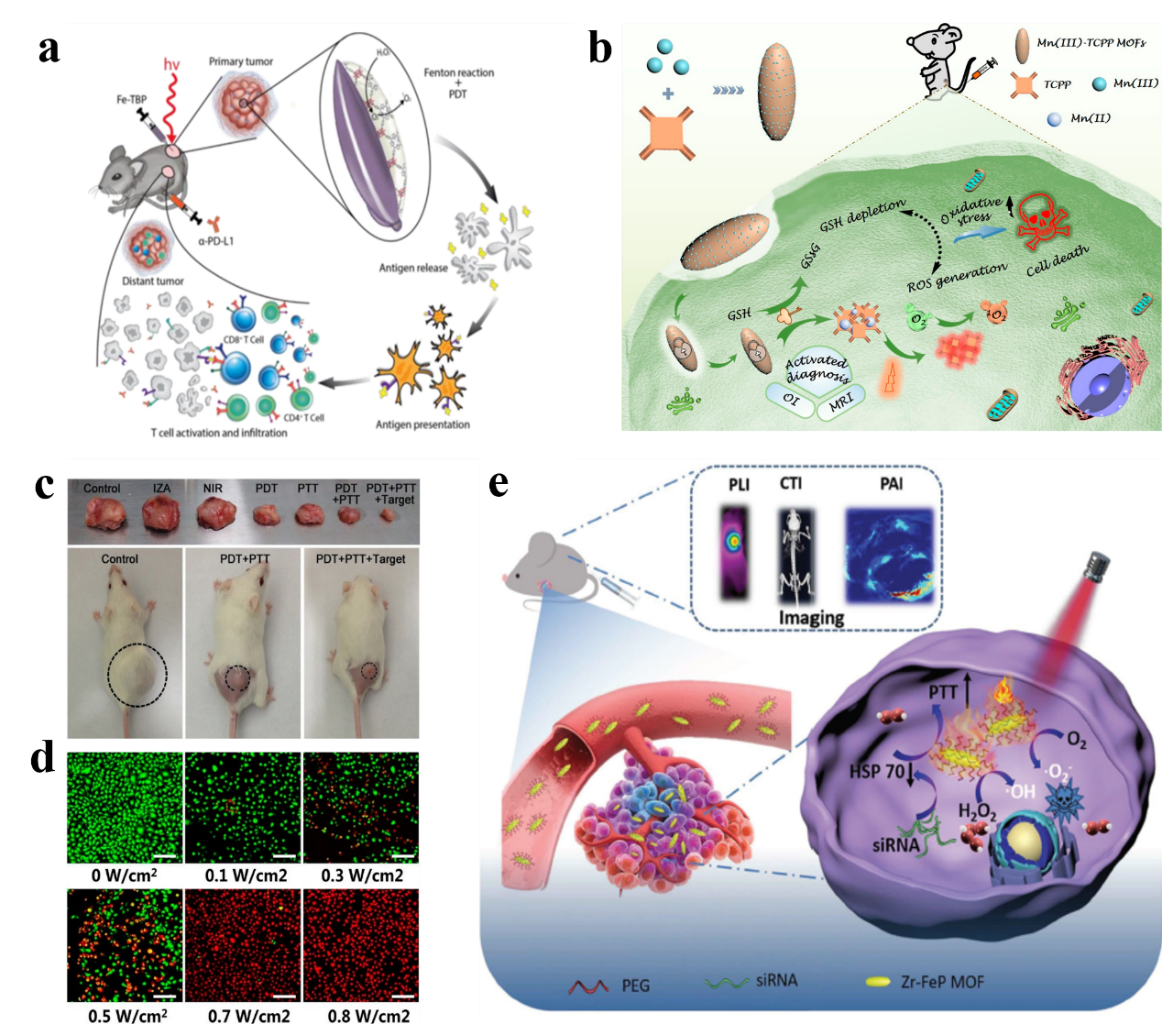
图3. NMOFs在光热及光动力治疗中的应用。
2.放疗
放疗是利用电离辐射与肿瘤组织之间的相互作用来破坏癌细胞中的DNA双链,达到肿瘤杀伤效果。然而,肿瘤组织对电离辐射能的特异性吸收不足,肿瘤微环境(如乏氧)对辐射产生的抵抗皆限制了放疗效果。NMOFs,由于具有较大的比表面积和周期性多孔结构,能有效负载放疗增敏剂,且利用重原子序数的元素对二次光子和电子经历非弹性散射,可显著提高放疗效率。同时,通过NMOFs对肿瘤微环境的调节,可有效减弱放疗抵抗,实现协同增效。放动力治疗作为放疗的补充,可通过选用卟啉及其衍生物作为配体,与重原子序数的离子(如Hf)配位来构建NMOFs基放疗增敏剂,实现肿瘤的放疗-放动力治疗。
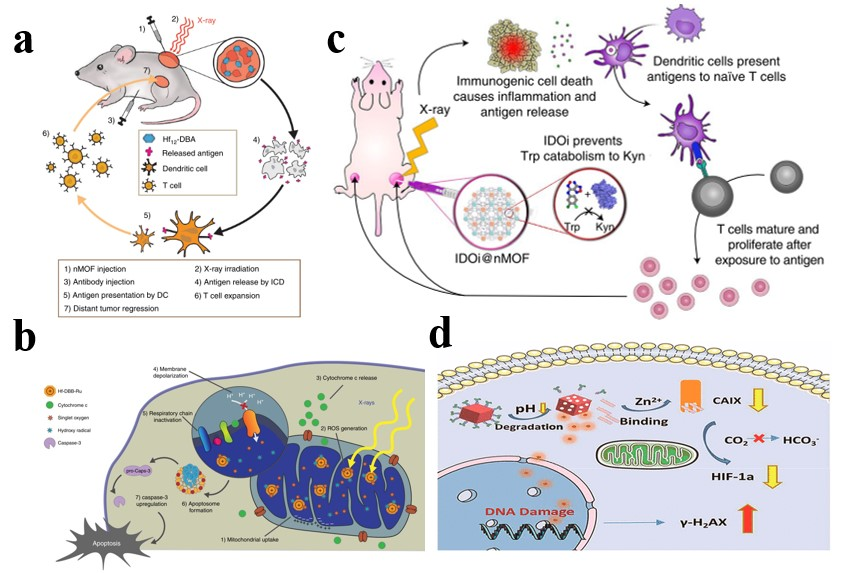
图4. NMOFs在放疗中的应用。
3. 微波治疗
微波具有热转换效率高、组织穿透深度深、不受气体和骨骼干扰等优势,是临床上常用的一种辐照源。肿瘤微波治疗主要包括微波热疗和微波动力疗法。微波热疗是通过将电磁场中极性分子产生的动能转化为热能,使肿瘤组织温度迅速升高,进而引起肿瘤细胞的坏死消融。微波动力是利用微波刺激增敏剂产生ROS,与肿瘤细胞发生氧化反应,诱导细胞凋亡或坏死。NMOFs由于具有纳米框架的限域效应,使得孔隙中聚集的离子在微波辐射下发生高频碰撞,从而将微波电磁能转化为热能。同时,NMOFs的多孔性及表面多活性位点可负载多种微波增敏剂(如离子液体等),从而实现肿瘤的微波热疗与微波动力治疗。
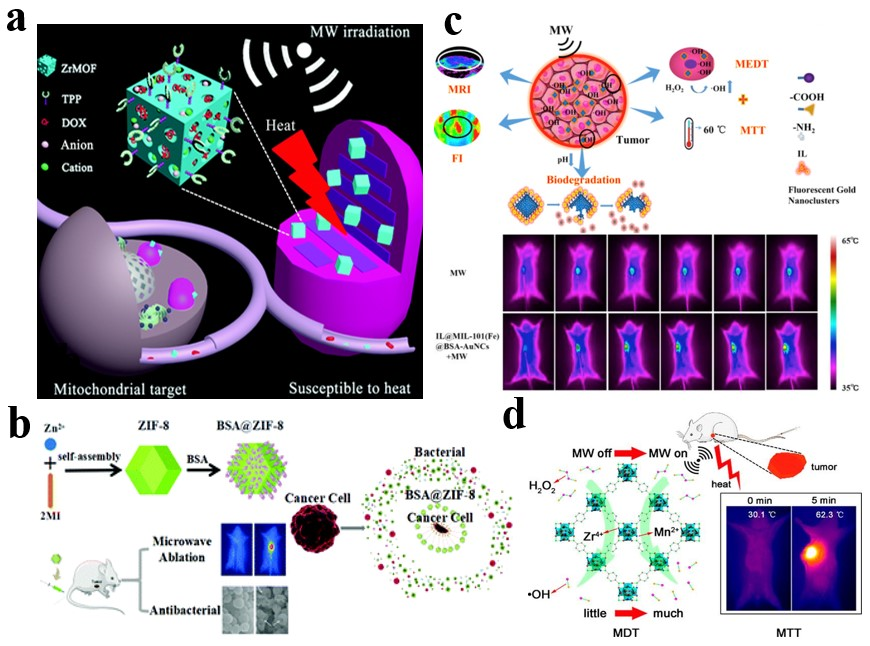
图5. NMOFs在微波治疗中的应用。
4. 声动力治疗
超声作为一种生物相容性好、对组织穿透深度深的机械波,已被广泛应用于肿瘤的临床治疗。高强度聚焦超声(HIFU)和声动力治疗(SDT)作为新型的超声治疗技术已被逐渐用于肿瘤治疗研究。SDT是依赖于超声辐射下声敏剂存在的一种无创疗法。NMOFs的多孔性及表面存在的大量活性位点,使得其可偶联或装载声敏分子,构建出生物相容性良好的超声敏感性系统。同时,具有声敏性的卟啉及其衍生物可与金属离子配位形成NMOFs基声敏剂,直接用于声动力治疗中。
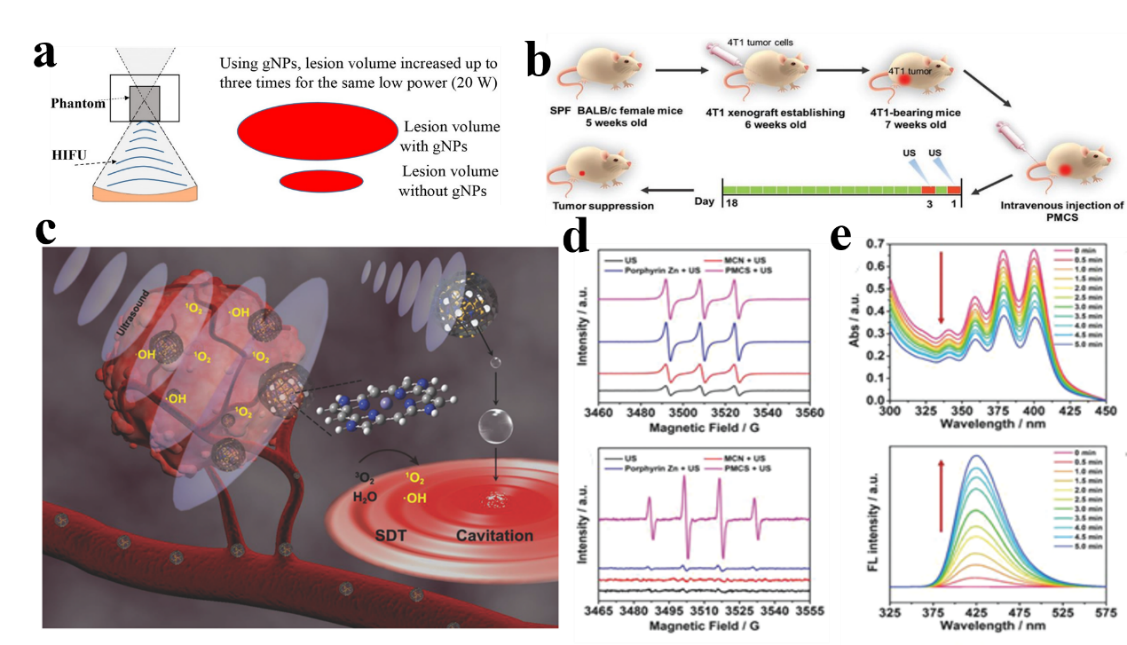
图6. NMOFs在声动力治疗中的应用。
总结与展望
1. NMOFs在肿瘤治疗中的相关研究
(1)NMOFs的合成条件多样化;
(2)NMOFs的生物相容性受尺寸、表面性质及形貌等影响;
(3)NMOFs既可作为纳米药物载体,又可作为荧光、MR、CT成像试剂;
(4)NMOFs在光疗、放疗、微波疗法及声动力治疗中,既是增敏剂良好的递送载体,又可通过各功能性金属或配体组装成独立的增敏系统。
2. NMOFs在临床转化前面临的问题
(1)对NMOFs进行可控制备,以获得合适尺寸、结构,且生物相容性好的NMOFs;
(2)NMOFs与细胞表面的相互作用,以及NMOFs的结构与治疗效率之间的关系;
(3)NMOFs在各疗法中的作用机制有待阐明;
(4)NMOFs需要进行更严格、更完善的临床前研究,包括急性毒性及分子水平上引起的亚慢性和慢性毒性评估。
NMOFs在生物医学领域的研究已启航,在临床转化中机遇与挑战并存!
参考文献
Li, S., Tan, L., Meng, X., NanoscaleMetal‐Organic Frameworks: Synthesis, Biocompatibility, Imaging Applications,and Thermal and Dynamic Therapy of Tumors. Adv. Funct. Mater.2020, 1908924.
https://doi.org/10.1002/adfm.201908924











