
第一作者:Min Liu, Yuanjie Pang,Bo Zhang, Phil De Luna
通讯作者:Edward H. Sargent
通讯单位:多伦多大学(加拿大)
通过电化学的方法我们能让吉布斯自由能变大于零的化学反应发生,让低自由能的物质转化为高自由能的物质,例如CO2 转化为 CO。通过电化学反应将CO2转化为CO是转化和利用CO2的重要反应,如何提高此反应的效率是一个非常重要的课题。
本文介绍的这篇2016年Edward H. Sargent发表在Nature上的研究工作,利用尖端离子富集的原理提高了CO2 转化为 CO 的电化学反应速率。文章中通过COMSOL进行了有限元模拟,计算了尖端的电化学反应过程,得到了电极附近的离子分布和电极表面的电流密度,充分阐述了尖端离子富集的物理机制。
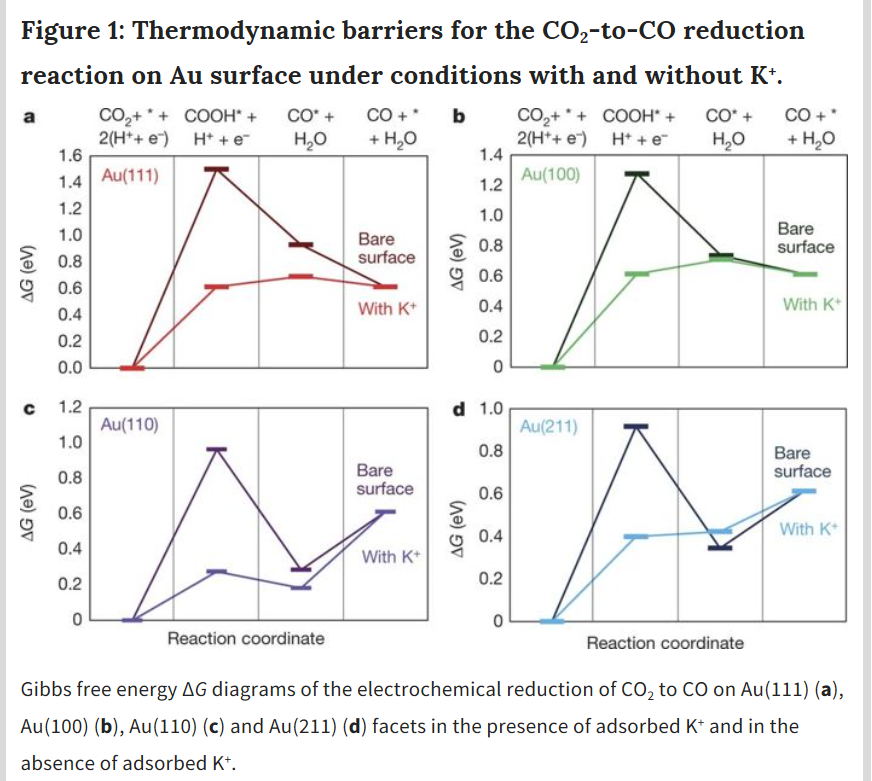
如图1所示,钾离子在电极表面吸附能够降低CO2在金电极表面的反应势垒,提高化学反应速率。
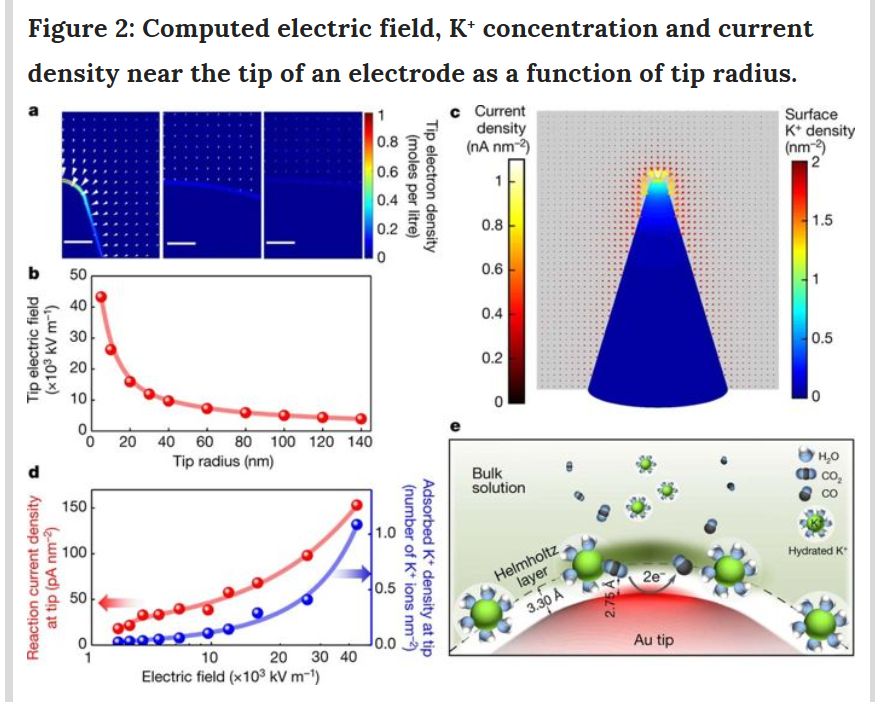
如图2所示,通过COMSOL 模拟计算得到电场和钾离子在空间中的分布以及表面电流密度。CO2在阴极表面发生还原反应,钾离子带正电荷能受到阴极的库仑吸引力吸附在电极表面形成扩散双电层。在电极尖端钾离子浓度会更高,表面电流密度也更大。电极表面曲率越小这种富集效果越强。
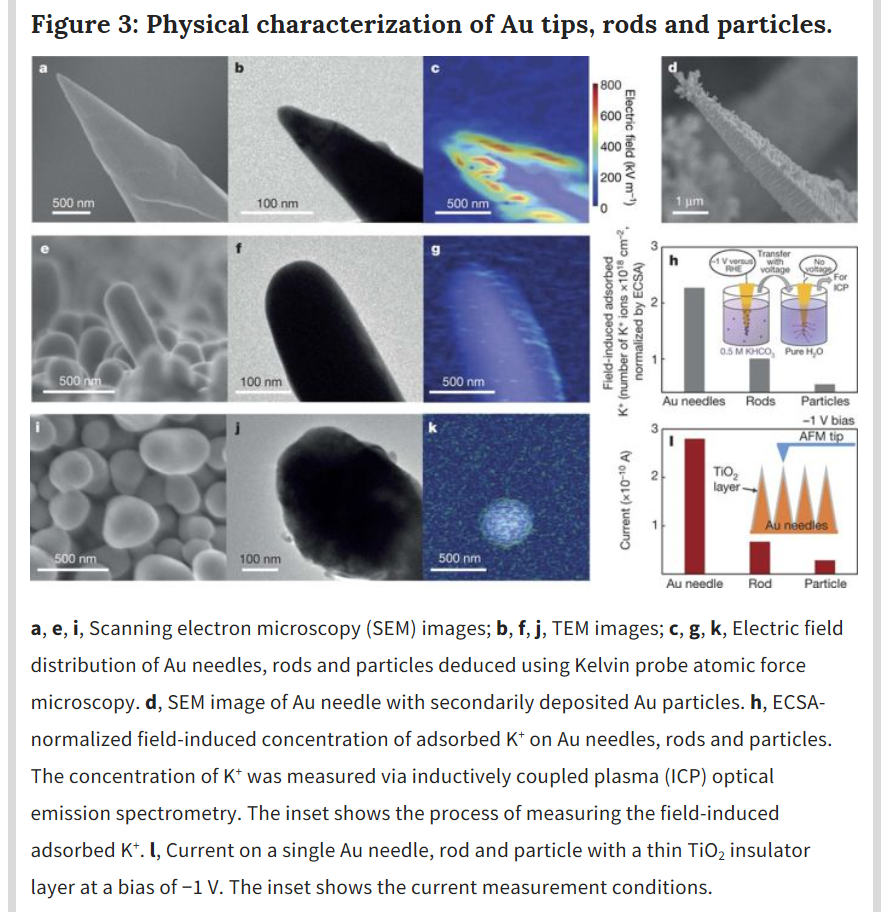
如图3所示,尖锥纳米金、棒状纳米金和颗粒纳米金的合成与表征。
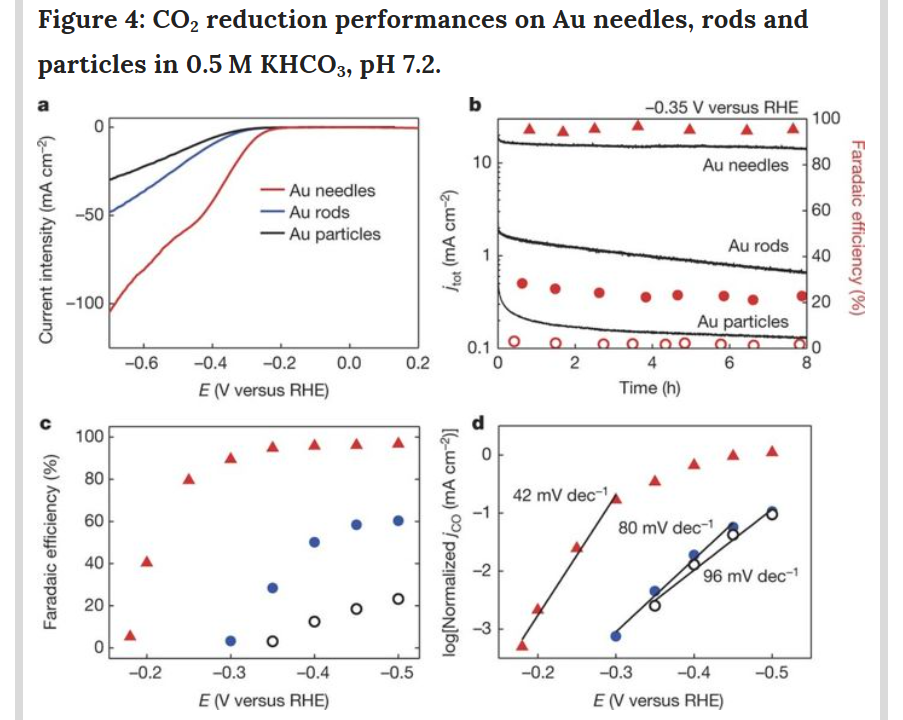
如图4所示,尖锥纳米金、棒状纳米金和颗粒纳米金在0.5M KHCO3溶液中催化CO2 还原的效果对比。尖锥纳米金的催化效果要远好于棒状纳米金和颗粒纳米金,因为尖端曲率更显钾离子富集效果越强,降低了的CO2反应的能垒。
总之,此工作合成了尖锥状的纳米金电极,并且发现通过此电极能极大提高CO2的反应速率。通过充实的理论分析,文章解释了钾离子在电极表面吸附能降低CO2反应的能垒,提高反应速率。另外模拟了尖锥状的纳米金电极表面的电化学反应过程,通过模拟的图像清楚的展示了尖端离子富集的机制。
Enhancedelectrocatalytic CO2 reduction via field-induced reagent concentration[J]. Nature, 2016, 537, 382.
电化学模拟的基本原理概述:
电化学反应的模拟会涉及到多个物理过程,包括物质扩散,带点离子在电场中的迁移和电极表面的化学反应。
描述电场下的物质扩散行为要在单纯的对流扩散方程(1)的基础上增加电场对带电离子的影响,也就是Nernst-Planck方程。如果要更精确的模拟离子的分布还需要考虑带点离子对电场的影响,这是时候需要把Nernst-Planck方程与泊松方程联立起来求解。我们把方程(2)(3)的联立成为Nernst-Planck-Poisson方程。通过求解Nernst-Planck-Poisson方程我们可以模拟离子在一个带电表面附近的浓度分布。一个经典的问题就是扩散双电层问题。通过COMSOL模拟扩散双电层能得到与经典理论Gouy–Chapman–Stern 模型一致的结果。
另外对于电极表面的化学反应通常使用Buler-Volmer方程进行计算。在给定外加电势和电极反应的平衡电势的条件下,通过Buler-Volmer方程能计算表面电流密度。

通过有限元模拟软件COMSOL,我们可以非常方便的实现电化学问题的模拟。COMSOL中提供了预置的接口,可以直接基于Nernst-Planck方程Nernst-Planck-Poisson方程和Butler–Volmer方程建模。充分利用COMSOL的优势能够极大的帮助我们的科研工作。











