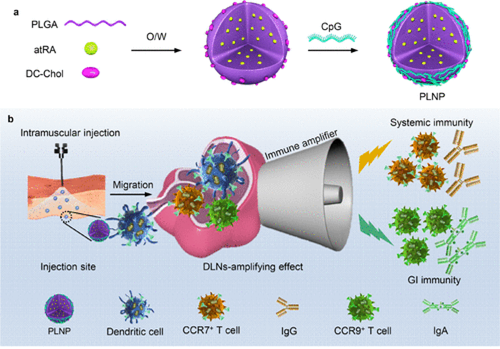
肠胃外疫苗接种不能同时引发有效的全身和胃肠道免疫保护,因为淋巴细胞通常限制于初免组织。尽管据报道全反式维甲酸(atRA)触发免疫细胞的肠归巢,但其生物利用度和全身性免疫应答仍然有限,无法用于坚固的肠道疫苗接种。因此,江南大学高晓冬教授联合中科院过程工程研究所吴颉研究员和马光辉研究员课题组通过共同递送atRA,CpG寡聚脱氧核苷酸(CpG)和抗原的工程化聚合物/脂质纳米颗粒(PLNP),并利用其引流淋巴结(DLN)的放大功能,实现强大的肠道嗜性和免疫激活。肌肉内注射后,在注射部位形成免疫增强的环境,PLNPs诱导引发的树突状细胞(DCs)转移到DLN而不是胃肠道组织的指定转移。在DLN中,免疫增强的环境显著放大了免疫细胞之间的抗原呈递和归巢受体转换,这同时刺激了外周和胃肠组织中活化淋巴细胞的优先耗散,即发挥了DLN放大作用。与目前的含atRA的制剂相比,PLNP不仅增强了外周组织中有效的IgG分泌和T细胞活化,而且还激发了卵清蛋白和EV71疫苗接种后胃肠道中强大的T细胞归巢和抗原特异性IgA水平。这些数据表明,利用DLN扩增可以刺激有效的全身和胃肠道反应,从而更有效地进行肠道疫苗接种
Du, Y.; Xia, Y.; Zou, Y.; Hu, Y.; Fu, J.; Wu, J.; Gao, X.-D.; Ma, G., Exploiting the Lymph-Node-Amplifying Effect for Potent Systemic and Gastrointestinal Immune Responses via Polymer/Lipid Nanoparticles. ACS Nano2019.
https://pubs.acs.org/doi/10.1021/acsnano.9b04071


















