传统的分子化疗药物和显像剂因为会被快速代谢清除,表现出相对较低的生物利用度,在细胞系统内实现药物的激活可能实现靶向治疗效果。在此,赵宇亮院士研究团队结合了成像探针和治疗方法,构建了一个肿瘤选择性级联激活自滞留系统(TCASS),并揭示其在肿瘤部位有效积累和滞留的机制,分析该系统的药代动力学。不同的小鼠模型中显示, TCASS系统在实体肿瘤中积聚。通过识别诱导的自组装效应,这些分子在肿瘤区域显示出增强的积累。对肿瘤组织中分子穿透的分析表明,与典型的软、硬纳米材料相比,体内自组装提高了穿透能力。重要的是,体内自组装的分子表现出与小分子相当的清除途径,小分子从网状内皮系统的器官(肝脏和肾脏)中排出,而相对缓慢地从肿瘤组织中清除。最后,该系统与近红外探针相结合,对于在分离的完整患者膀胱中检测膀胱癌显示出高度的特异性和敏感性。
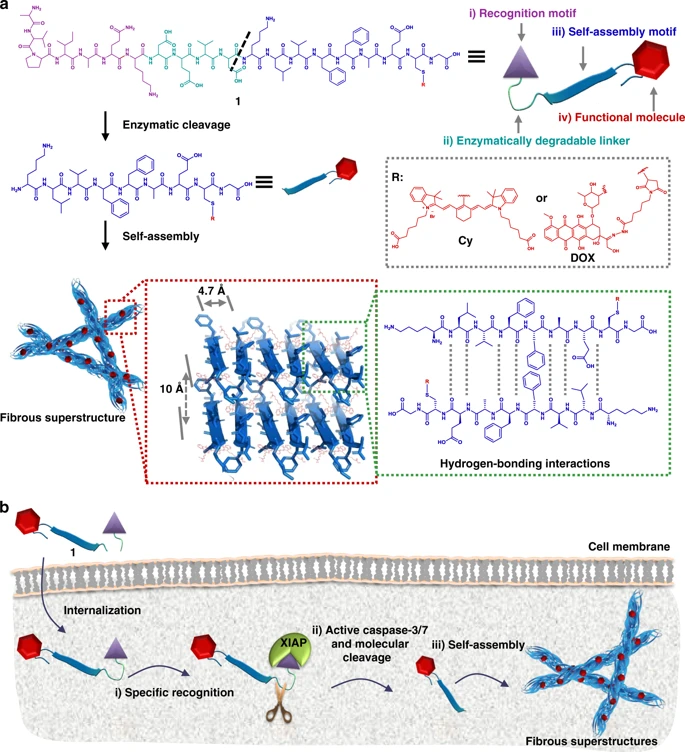
Hong-Wei An, Li-Li Li, Yi Wang, et al. A tumour-selective cascade activatable self-detained system for drug delivery and cancer imaging. Nat. Commun., 2019.
https://doi.org/10.1038/s41467-019-12848-5


















