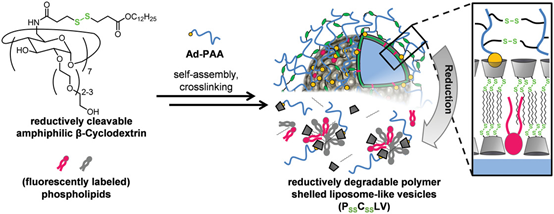
两亲性化合物如荧光标记的磷脂向细胞的特异性转运是分析涉及这些分子的高动态细胞过程(如:磷脂的细胞内分布和代谢)的先决条件。但是,在细胞传递过程中,由于不能影响细胞膜的生理完整性和形态,所以细胞传递仍然是一个挑战。为了解决这个问题,德国明斯特大学Volker Gerke教授和Bart Jan Ravoo教授课题组制备了基于氧化还原反应性环糊精(CD)两亲物的聚合物纳米容器,并分析了其将荧光标记的磷脂传递到细胞内膜区室的能力。结果表明,可还原降解的环糊精两亲物和不同磷脂的混合物形成类脂质体囊泡(CD-脂质囊泡,CSSLV),每种脂质都均一分布。在这些CSSLV上由主客体介导自组装的胱胺交联的聚合物壳生成了具有独特功能的聚合物壳脂质体囊泡(PSSCSSLV),即PSSCSSLV具有氧化还原敏感CSSLV核和可还原降解的聚合物壳。PSSCSSLV具有高稳定性和氧化还原敏感释放两亲性载体特性。活细胞实验表明,新型PSSCSSLV易于被原代人内皮细胞内化,并且细胞内体的还原性微环境触发了两亲性物质释放到细胞质中。因此,PSSCSSLV成为一种可将类脂质的两亲性物质运输到细胞内环境中的高效的载体系统。
Vries, W. C., Kudruk, S., Grill, D., Niehues, M., Matos, A. L. L., Wissing, M., Studer, A., Gerke, V.,Ravoo, B. J., Controlled Cellular Delivery of Amphiphilic Cargo by Redox‐Responsive Nanocontainers. Adv. Sci. 2019, 1901935.
https://doi.org/10.1002/advs.201901935


















