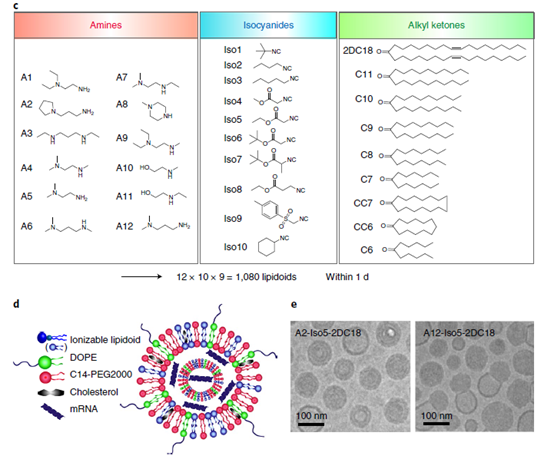
治疗性信使RNA疫苗可以递送完整抗原,这比肽疫苗更具优势。然而,最佳疗效既需要细胞内递送以允许抗原翻译,又需要适当的免疫激活。于此,生物材料鼻祖麻省理工大学Robert Langer教授和Daniel G. Anderson教授共同指导开发了可电离的类脂质材料的组合库,以鉴定可促进在体内的mRNA递送并提供有效和特异性免疫激活的mRNA递送载体。使用三维多组分反应系统,研究人员合成并评估了1,000多种脂质制剂的疫苗潜力。最佳的制剂可诱发强烈的免疫反应,并能够抑制肿瘤生长并延长黑色素瘤和人乳头瘤病毒E7体内肿瘤模型的生存期。表现最佳的脂质有一个共同的结构:不饱和脂质作为尾部、二氢咪唑基作为连接部和环状胺基团作为头部。这些制剂通过细胞内干扰素基因刺激因子(STING)途径的而不是通过Toll样受体诱导抗原呈递细胞成熟,并导致有限的全身细胞因子表达和增强抗肿瘤功效。
Miao, L.; Li, L.; Huang, Y.; Delcassian, D.; Chahal, J.; Han, J.; Shi, Y.; Sadtler, K.; Gao, W.; Lin, J.; Doloff, J. C.; Langer, R.; Anderson, D. G., Delivery of mRNA vaccines with heterocyclic lipids increases anti-tumor efficacy by STING-mediated immune cell activation. Nature Biotechnology 2019, 37 (10), 1174-1185.
https://doi.org/10.1038/s41587-019-0247-3


















