核酸无论是作为遗传蓝图还是作为各种生化途径的调节剂,在生命科学的各个领域都扮演着核心角色。在此,北卡罗来纳大学夏洛特分校Kirill A. Afonin研究团队对核酸适体作为治疗性纳米技术在生物医学领域的应用进行了综述。核糖核酸(RNA)或脱氧核糖核酸(DNA)通常由四个单体的序列组成,为生物聚合物的折叠和高阶组装提供了精确的指令,进而决定了生物功能。基于序列的特定三维结构的核酸导致了针对所选目标分子的寡核苷酸的定向进化,即SELEX(通过指数富集配体的系统进化)。在众多功能中,被选为适体的寡核苷酸还可以像抗体一样精准靶向细胞特异性受体,并且可以在没有转染剂的条件下传递功能性RNA。可定制核酸纳米颗粒(NANPs)领域的进展为利用适体触发或阻断细胞信号通路或利用适体-受体组合激活治疗功能的纳米组装体的设计开辟了道路。最新报道的荧光适体能够实时跟踪NANP的形成和相互作用,表明适体有望为未来技术的发展做出贡献,使功能性NANP能够在哺乳动物细胞或体内高效组装。这些研究课题对于治疗性核酸纳米技术领域至关重要,有望大规模生产适合生物医学应用的NANP,控制生物材料的胞内组织以提高生化途径的效率,并增强基于NANP疗法的治疗潜力,同时最大限度减少不良副作用和毒性。
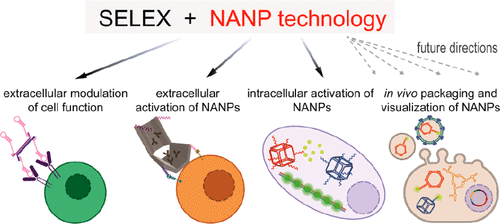
Martin Panigaj, M. Brittany Johnson, Weina Ke, et al. Aptamers as Modular Components of Therapeutic Nucleic Acid Nanotechnology. ACS Nano, 2019.
https://doi.org/10.1021/acsnano.9b06522


















