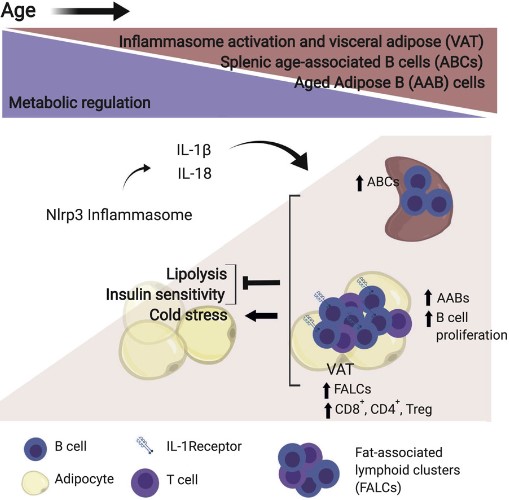
在衰老过程中,内脏脂肪通常与脂肪组织(AT)白细胞改变、炎症和代谢功能障碍有关。然而,衰老过程中AT B细胞在免疫代谢中的作用仍未阐明。近日,美国耶鲁大学Vishwa Deep Dixit的研究团队,发现衰老诱导脂肪B细胞Nlrp3炎性小体依赖性扩张,并破坏代谢稳态。研究人员发现衰老与在脂肪相关淋巴样簇(FALCs)中发现的特异驻留非衰老老年脂肪B细胞(AAB)的扩张有关。AAB在转录上不同于脾脏年龄相关性B细胞(ABC),并在雌性小鼠中显示出更大的扩增。从功能上讲,全身B细胞耗竭可在冷应激期间恢复适当的脂解作用和维持核心体温。从机理上讲,年龄引起的FALC形成、AAB和脾脏ABC扩张取决于Nlrp3炎性体。此外,AAB表达IL-1R并且抑制IL-1信号传导,这会减少其增殖并增加衰老过程中的脂解作用。这些数据表明抑制Nlrp3依赖的B细胞积累可以靶向逆转衰老AT的代谢损伤。
Christina D. Camell, Patrick Günther, Aileen Lee, et al. Aging Induces an Nlrp3 Inflammasome-Dependent Expansion of Adipose B Cells That Impairs Metabolic Homeostasis. Nature, 2019.
DOI: 10.1016/j.cmet.2019.10.006
https://www.cell.com/cell-metabolism/fulltext/S1550-4131(19)30561-3


















