肿瘤血管系统在维持肿瘤生长中起关键作用。血管破裂伴随着内部凝血,血小板的聚集和由此产生的氧供应的抑制。在此,武汉大学张先正和冯俊研究团队人为创建了这一生理过程,以建立血管中断和模拟血小板的生物趋化之间的相互反馈,用于缺氧依赖治疗的级联扩增。为了证明这一概念,将介孔二氧化硅纳米颗粒与缺氧激活的前药(HAP)和血管破坏剂共负载,然后涂覆血小板膜。一旦进入肿瘤,此纳米疗法可以破坏局部血管从而抑制肿瘤。这种血小板膜包覆的纳米平台与亲代血小板共享出血倾向性功能,并且可以被血管破裂的肿瘤持续聚集。通过这种方式,肿瘤内血管破裂和肿瘤靶向在生物学上是相互依赖和相互加强的。依靠这种相互反馈,肿瘤缺氧被极大地促进了20倍以上,说明了HAP的细胞毒性得到了有效恢复。因此,此受生物启发的纳米设计通过肿瘤内血管破裂、模拟血小板的生物趋化、级联低氧扩增和低氧敏感化疗之间的生物驱动合作,表现出高度特异性和有效的抗肿瘤效力。这项研究提供了将治疗设计与生理事件相关联以实现更好的治疗效果的范例。
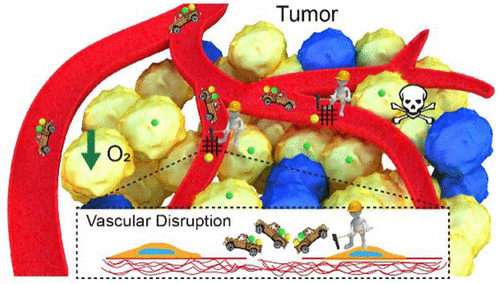
Mingkang Zhang, Jing-Jie Ye, Yu Xia, et al. Platelet-Mimicking Biotaxis Targeting Vasculature-Disrupted Tumors for Cascade Amplification of Hypoxia-Sensitive Therapy. ACS Nano, 2019.
https://doi.org/10.1021/acsnano.9b07330


















