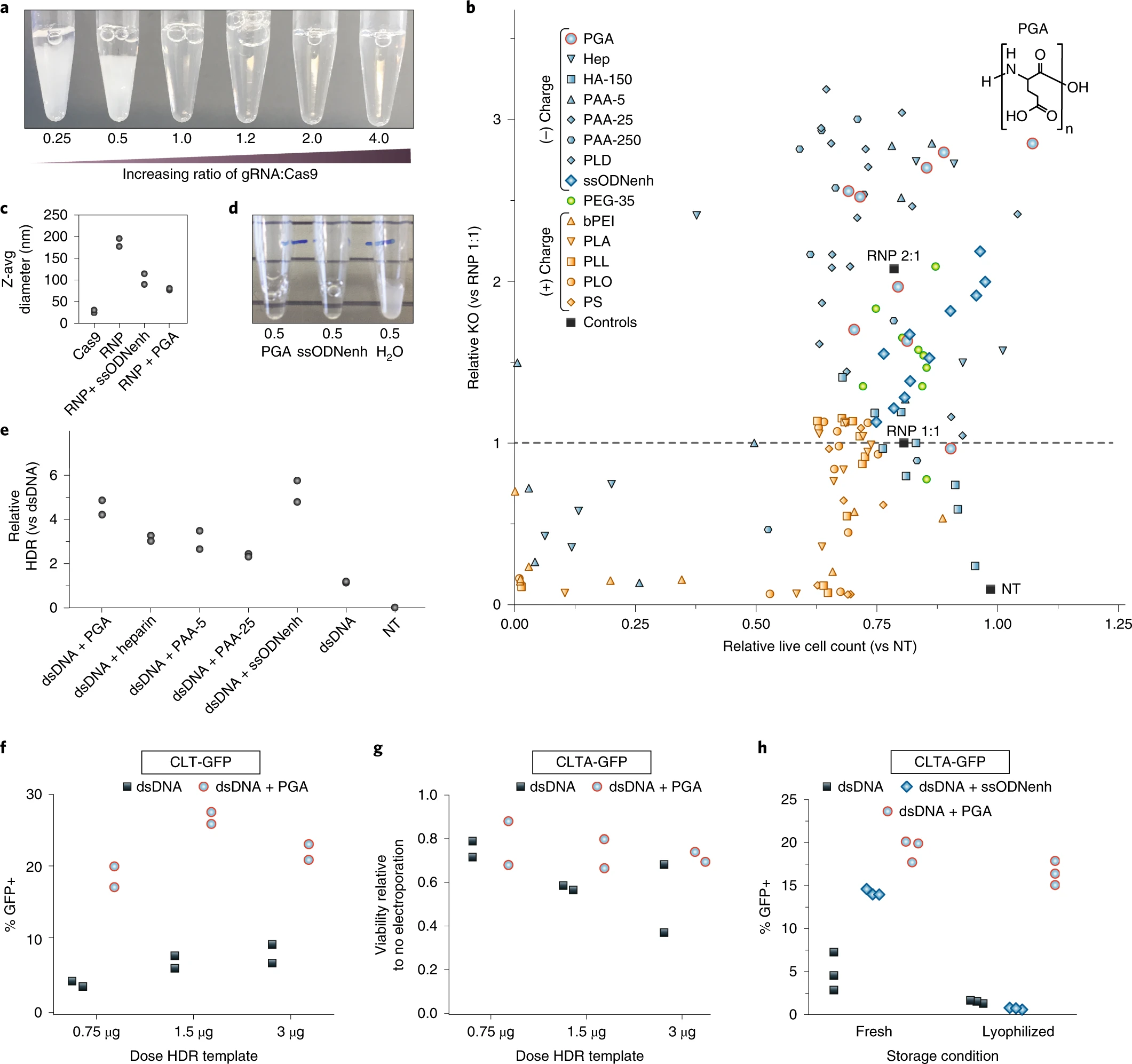
需要多种多样且精确的基因组修饰来创建更广泛的过继细胞疗法。于此,美国加州大学旧金山分校Alexander Marson教授等人两种提高临床相关原代细胞类型中基于CRISPR-Cas9的基因组编辑效率的改进。在同源介导的双链DNA修复(HDR)模板末端添加的截短的Cas9靶序列(tCTSs)与Cas9核糖核蛋白(RNP)相互作用,用以将模板穿梭至细胞核,从而将HDR效率提高了约2-4倍。此外,用聚谷氨酸将Cas9 RNP稳定在纳米颗粒中,可进一步提高编辑效率约两倍,降低毒性,并能冻干保存而不损失活性。结合这两种改进,即使在减少的HDR模板剂量下,也能提高基因打靶效率,使得在不同的细胞类型中产生多个基因位点的约两到六倍的可编辑细胞,如Buck(CD3+)T细胞、CD8+T细胞、CD4+T细胞、调节性T细胞(Treg)、γδT细胞、B细胞,自然杀伤细胞,原代和诱导多能干细胞衍生造血干祖细胞(HSPC)。
Nguyen, D.N., Roth, T.L., Li, P.J. et al. Polymer-stabilized Cas9 nanoparticles and modified repair templates increase genome editing efficiency. Nat Biotechnol (2019)
doi:10.1038/s41587-019-0325-6
https://doi.org/10.1038/s41587-019-0325-6


















