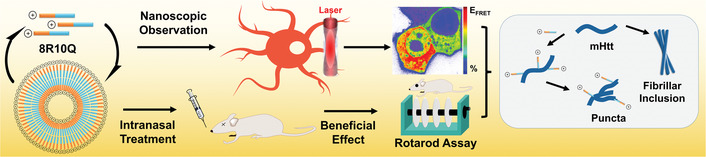
寻找一种有效的治疗方案是包括亨廷顿病(HD)在内的各种神经退行性疾病的迫切需要。由于难以观察到体内突变亨廷顿蛋白(mHtt)的动态聚集和寡聚过程,在分子蛋白水平上对潜在药物的评价往往会受到限制。通过结合基于寿命的荧光显微镜和生物物理工具,台湾中央研究院Joseph Jen‐Tse Huang、Ruei‐Yu He及Pang‐Hsien Tu研究团队发现一种设计的两亲性肽,其在早期以mHtt为靶点,可以纳米尺度上干扰寡聚体的组装过程,抑制mHtt的淀粉样属性,在构象上转变mHtt的寡聚体和/或聚集体,并改善mHtt诱导的细胞和HD小鼠模型中神经损伤和聚集。研究还发现,这种两亲性多肽能够通过鼻腔给药转运到大脑并修复记忆障碍,表明其在体内具有靶向性。综上所述,本研究提供了一个生物光子平台来详细研究寡聚/聚集过程,从而为亨廷顿病靶向治疗剂的设计和效果提供了思路。
Ruei‐Yu He, Xiang‐Me Lai, Chia‐Sui Sun, et al. Nanoscopic Insights of Amphiphilic Peptide against the Oligomer Assembly Process to Treat Huntington's Disease. Adv. Sci., 2019.
https://doi.org/10.1002/advs.201901165


















