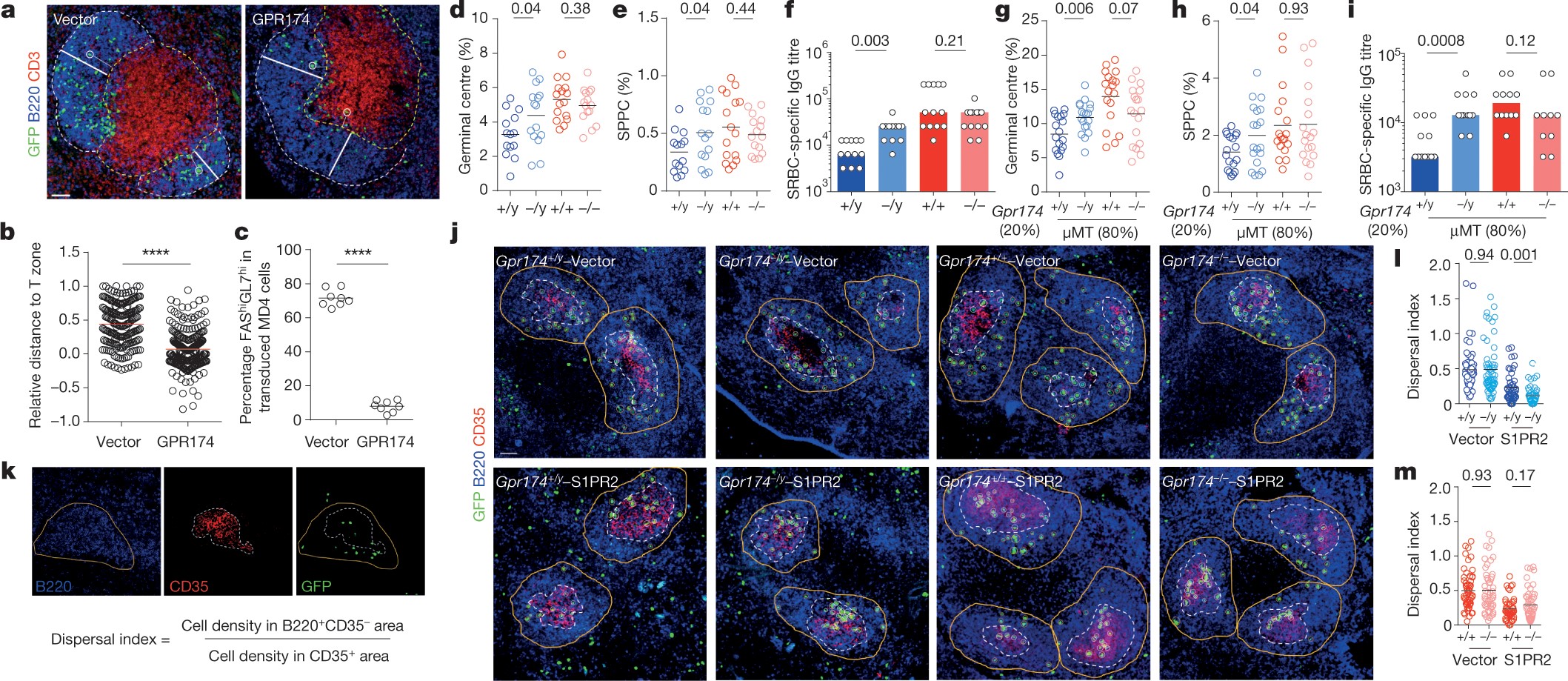
男性对免疫和感染的体液免疫反应以及对抗体介导的自身免疫的敏感性较低。但是,这种性别二态性的潜在机制尚未得到很好的理解。近日,清华大学祁海团队,发现GPR174-CCL21模块影响体液免疫应答的两性差异。研究人员表明,在雄性和雌性小鼠中产生生发中心的B细胞之间存在内在差异。研究人员发现,抗原激活的雄性B细胞不能像雌性B细胞那样有效地将自己定位在次生淋巴器官的滤泡中心(这是生发中心发育的地方)。此外,GPR174是一种X染色体编码的G蛋白偶联受体,可抑制雄性小鼠(而非雌性小鼠)生发中心的形成。这种效应是B细胞所固有的,并且与GPR174增强的B细胞朝向滤泡的T细胞-B细胞边界的位置相关,此外与雄性而非雌性B细胞从S1PR2驱动的滤泡中心定位中分散开来有关。以GPR174依赖性方式诱导B细胞迁移的条件培养基的生化分离可确定CCL21为GPR174配体。响应CCL21,GPR174触发钙流并优先诱导雄性B细胞迁移。与雌性B细胞相比,雄性中GPR174还与更多的Gαi蛋白相关。摘除睾丸的小鼠的雄性B细胞表现出受损的GPR174介导的向CCL21的迁移,而睾丸激素治疗可以挽救这一缺陷。睾丸激素处理过小鼠的雌性B细胞表现出类似雄性的GPR174–Gαi缔合和GPR174介导的迁移。从雄性B细胞中删除GPR174导致更有效地定位于滤泡中心,形成更多的生发中心,并增加了对B细胞依赖性实验性自身免疫性脑脊髓炎的敏感性。通过鉴定GPR174作为CCL21的受体,并证明了其对B细胞定位和参与生发中心的性别依赖性控制,研究人员揭示了一种机制,即通过该机制来微调B细胞生理,以赋予体液免疫性别二态性。
Ruozhu Zhao, Xin Chen, Weiwei Ma, et al. A GPR174–CCL21 module imparts sexual dimorphism to humoral immunity. Nature, 2019.
DOI: 10.1038/s41586-019-1873-0
https://www.nature.com/articles/s41586-019-1873-0


















