主动肿瘤靶向是指在纳米材料上修饰噬癌载体生物分子,这些生物分子可选择性地识别恶性肿瘤细胞或肿瘤微环境中的某些抗原。这一策略可以通过受体介导的内吞作用等特异性相互作用促进细胞内纳米材料的摄取,并可以通过阻止其从肿瘤快速外排而延长纳米材料在恶性肿瘤组织中的滞留时间。在此,德国HZDR研究院Holger Stephan、Kristof Zarschler等人设计了一种用于癌症诊断成像的主动靶向,肾脏可排泄的双峰树突状聚甘油(dPGs)。其中与表皮生长因子受体(EGFR)特异性结合的单域抗体(sdAbs) 因其体积小,与相应抗原的亲和力高而被作为靶向弹头。根据体外与EGFR过表达细胞的相互作用以及体内受体阳性肿瘤的积聚,将具有EGFR靶向功能的dPGs与非靶向dPGs进行面对面的比较。实验结果表明,α-EGFR dPGs具有更高的特异性和优先的肿瘤聚集,这是由于在其主干上引入了主动靶向能力。这些结果突出了sdAb功能化策略在改善dPGs的肿瘤摄取特性的潜力,表明对开发具有高度特异性肿瘤积累特性的超小纳米材料的发展是有用的。
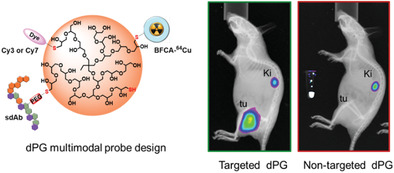
Kritee Pant, Christin Neuber, Kristof Zarschler, et al. Active Targeting of Dendritic Polyglycerols for Diagnostic Cancer Imaging. Small, 2019.
https://doi.org/10.1002/smll.201905013


















