在战斗或逃跑反应期间心脏收缩力的增加是由通过CaV1.2电压门控钙通道的β-肾上腺素能增加来实现的。然而,这种增加在表达突变型CaV1.2α1C和β亚基的转基因小鼠心脏中仍然存在,由于这些突变不能被蛋白激酶A(一种β肾上腺素信号传导的重要下游介质)磷酸化,从而表明这种增加还需要非通道因子。近日,美国哥伦比亚大学Steven O. Marx、哈佛医学院Marian Kalocsay等研究人员,揭示了β-肾上腺素能激动剂刺激电压门控钙通道的机制。研究人员在小鼠心脏中表达与抗坏血酸过氧化物酶5偶连的α1C或β2B亚基,并使用多重定量蛋白质组学来跟踪CaV1.2附近的数百种蛋白质。研究人员观察到钙通道抑制因子Rad(一种单体G蛋白),在CaV1.2微环境中富集,但在β-肾上腺素刺激过程中被耗尽。蛋白激酶A对Rad上特定丝氨酸残基的磷酸化作用降低了其对β亚基的亲和力,并减轻了CaV1.2的组成型抑制作用,这被视为通道开放可能性的增加。Rad或其同源物Rem在HEK293T细胞中的表达也可通过蛋白激酶A刺激CaV1.3和CaV2.2,从而揭示了进化保守的机制,即可在电压门控钙通道上赋予肾上腺素调节能力。
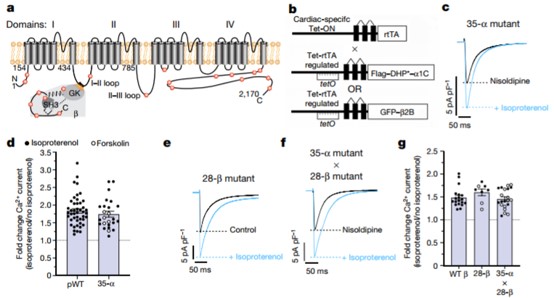
Guoxia Liu, Arianne Papa, Alexander N. Katchman, et al. Mechanism of adrenergic Ca V 1.2 stimulation revealed by proximity proteomics. Nature, 2020.
DOI: 10.1038/s41586-020-1947-z
https://www.nature.com/articles/s41586-020-1947-z


















