纳米胶束以其优异的生物相容性、可降解性和对疏水性药物的增溶能力,已被广泛用作抗癌药物最有效的给药平台。然而,不理想的载药能力、不易修饰、体内稳定性差以及肿瘤内渗透等问题仍有待解决。有鉴于此,华东理工大学的Yuan Yuan、Changsheng Liu等研究人员,介绍了一种新型的核壳聚癸二酸甘油酯(PEGS)/羟基磷灰石(HA)杂化纳米胶束,该杂化纳米胶束是基于一种独特的三嵌段聚癸二酸甘油酯(PEGS)底物,其末端带有功能性羧基和游离羟基作为侧基。
本文要点
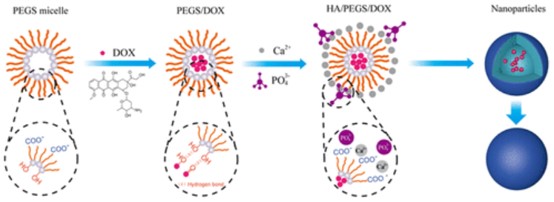
1)疏水性阿霉素(DOX)可以通过氢键可控地包裹在纳米胶束的核心,在羧酸根(COO-)和钙离子(Ca2+)之间的静电作用下,HA以壳层的形式原位矿化。
2)通过优化PEGS纳米胶束与HA矿化的配位,可以在相当大的载药量(0.38 mg DOX/1 mg纳米颗粒)和灵敏的pH响应释放(pH 5.6时约50%的释放量,而pH 7.4时24小时<5%的释放量)下制备出20-30 nm的球形纳米颗粒。
3)在进一步的体外研究中,这种PEGS/HA杂化纳米颗粒系统显示出优异的选择性肿瘤抑制效果,而在体内研究中,负载DOX的PEGS/HA组具有较高的抑瘤效果和较低的毒性发生率(皮下注射15天后,平均肿瘤体积比对照组减少71.7%)。
PEGS纳米微粒与PEGS纳米胶束配位和原位HA矿化具有高载药量、多功能性、肿瘤选择性和反应性释放等特点,为肿瘤治疗提供了一个极具前景的临床应用平台。
参考文献:
Zihan Wu, et al. Core/Shell PEGS/HA Hybrid Nanoparticle Via Micelle-Coordinated Mineralization for Tumor-Specific Therapy. ACS Applied Materials & Interfaces, 2020.
DOI:10.1021/acsami.0c00068
https://pubs.acs.org/doi/abs/10.1021/acsami.0c00068


















