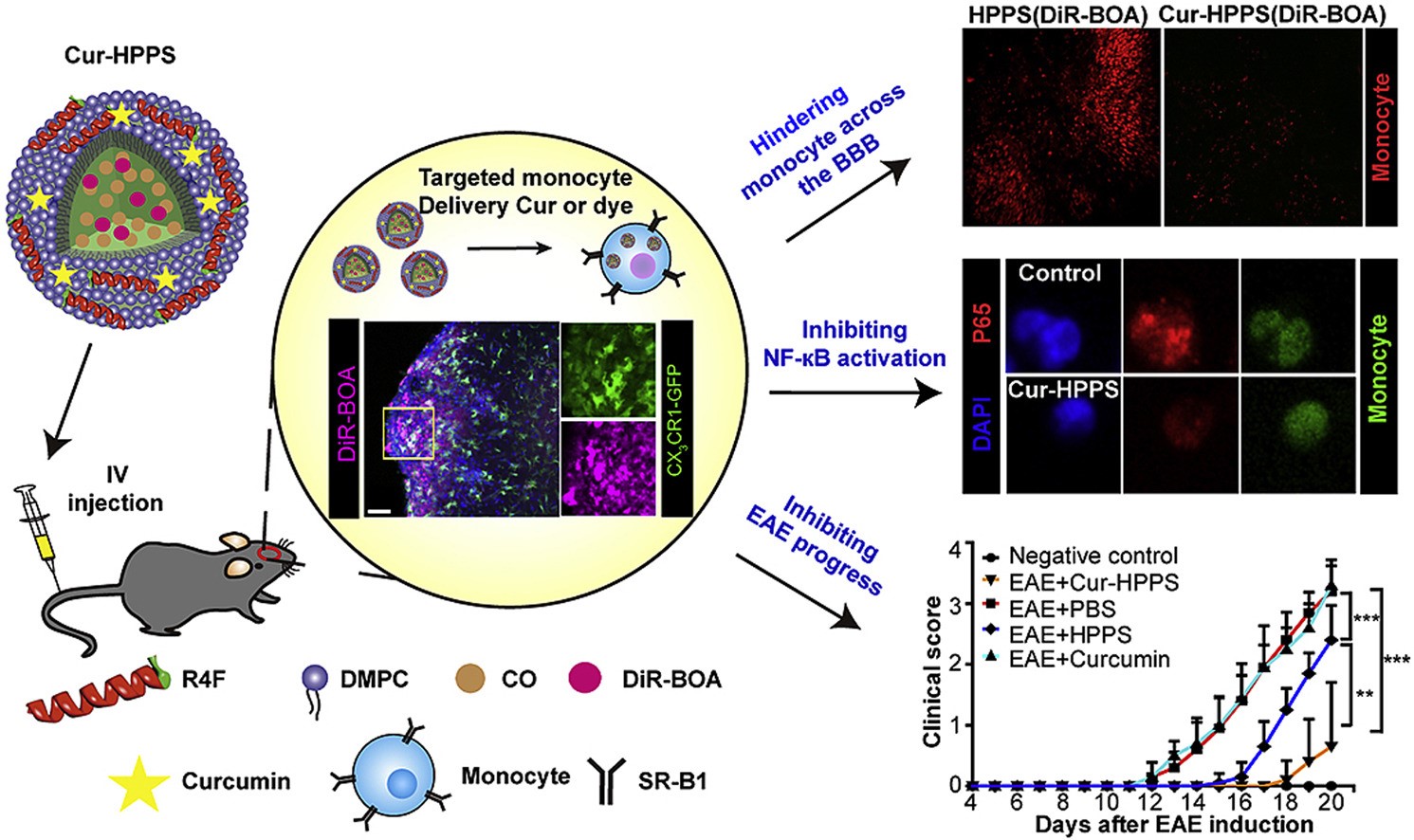
由于多种自身抗原引起的复杂发病机理,很难进行多发性硬化症(MS)的早期诊断和治疗。单核细胞在MS的过程中起重要作用,尤其是当大多数扩增的炎性单核细胞通过BBB促进神经元损伤并募集更多的免疫细胞渗入中枢神经系统(CNS)时。有鉴于此,华中科技大学Zhihong Zhang等研究人员,将单核细胞作为治疗MS的有效免疫靶点,采用高密度脂蛋白模拟肽-磷脂支架(HPPS)作为载体来提高姜黄素的生物利用度。
本文要点
1)姜黄素负载的HPPs(Cur-HPPs)通过清道夫受体BI型(SR-B1)被单核细胞特异性、高效地摄取。这种传递方式可阻止炎性单核细胞穿过EAE小鼠的血脑屏障,抑制小胶质细胞的增殖,并限制其他效应免疫细胞的浸润,从而使EAE的发病率从100%降至30%。
2)Cur-HPPs对炎症单核细胞具有免疫调节作用,抑制NF-κB活化,下调黏附和迁移相关分子的表达,可能是Cur-HPPs对炎性单核细胞的免疫调节作用。
3)同时,EAE小鼠中枢神经系统内浸润的单核细胞是早期炎症的特征。
因此,携带治疗性和/或显像剂的HPPs靶向调控单核细胞为MS的诊断和治疗提供了一种新的策略。
参考文献:
Lisen Lu, et al. Targeted immunomodulation of inflammatory monocytes across the blood-brain barrier by curcumin-loaded nanoparticles delays the progression of experimental autoimmune encephalomyelitis. Biomaterials, 2020.
DOI:10.1016/j.biomaterials.2020.119987
https://www.sciencedirect.com/science/article/pii/S0142961220302337


















