表征蛋白质相互作用对于理解其功能至关重要。最近,已证明基于单分子成像的方法可用于直接测试多亚基蛋白质复合物的化学计量。一个限制因素是具有多个光谱可识别标签且低背景的蛋白质标记。于此,德国弗莱堡大学Maximilian H. Ulbrich等人描述了锌指(ZF)介导的蛋白质标记在活细胞中进行单分子成像研究的用途。
本文要点:
1)将结合DNA的ZF融合到目标蛋白质上,并用带有特定ZF结合序列和有机染料的DNA探针标记。通过将DNA/染料偶联物注射到细胞中,可以将非特异性结合减至最小。
2)以20%的可复制标记效率,研究人员开发了一种从整体标记程度推论蛋白质复合物中亚基多样性的方法。且能够在三色单分子成像设置中确认NMDA受体的固定2:2组装,并拒绝其他化学计量。由于ZF蛋白的模块化设计和小尺寸,这种方法将允许分析更复杂的蛋白相互作用模式,以了解大蛋白复合物的组装规则。
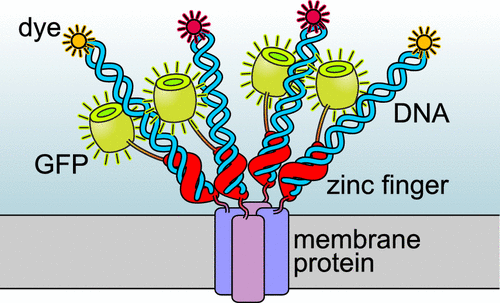
Changsheng Chen and Maximilian H. Ulbrich. Zinc-Finger-Mediated Labeling Reveals the Stoichiometry of Membrane Proteins. ACS Nano 2020.
DOI: 10.1021/acsnano.9b08865
https://doi.org/10.1021/acsnano.9b08865


















