用于体内的系统给药纳米颗粒(NPs)的快速肝和脾调理仍然是纳米医学的致命弱点,通常只允许一小部分材料到达预定的目标组织。虽然专注于疾病自然处置纳米颗粒的器官是一个可行的选择,但它限制了可能从纳米医学干预中受益的多种损伤。在此,美国华盛顿大学(圣路易斯)Samuel Achilefu等人设计了一个由二氧化钛(TiO2)纳米颗粒组成的纳米治疗平台,该平台包覆有肿瘤靶向剂转铁蛋白(Tf),并用放射性核素(89Zr)进行放射性标记,用于靶向骨髓, NPs的分布成像,并刺激ROS的产生以用于细胞杀伤。
本文要点:
1)用89Zr标记TiO2 NPs,可以在不改变纳米粒子形貌的情况下,获得热力学和动力学稳定的无螯合89Zr-TiO2-Tf NPs。
2)89Zr-TiO2-Tf治疗多发性骨髓瘤(MM)细胞(一种起源于骨髓的浆细胞疾病)会产生细胞毒性活性氧(ROS),通过凋亡途径诱导癌细胞杀伤。
3)正电子发射断层扫描/X射线计算机断层扫描(PET/CT)成像和组织生物分布研究表明,将89Zr-TiO2-Tf注射到小鼠体内,利用89Zr的趋骨作用,可以选择性地将大约70%的注射放射性物质定位在小鼠骨组织中。
4)研究NP分布的小动物PET/CT成像和癌症进展的生物发光成像联合显示,在弥漫性MM小鼠模型中,单剂量89Zr-TiO2-Tf治疗完全抑制了未治疗小鼠安乐死时的癌症生长,并至少使经治疗的小鼠的存活率增加了一倍。Zr-TiO2-Tf、89Zr-草酸盐或89Zr-Tf处理的小鼠与未处理的对照组相比没有任何疗效。这项研究揭示了一种有效的放射性核素敏化纳米光疗范例,用于治疗多发性骨髓瘤和其它可能与骨相关的恶性肿瘤。
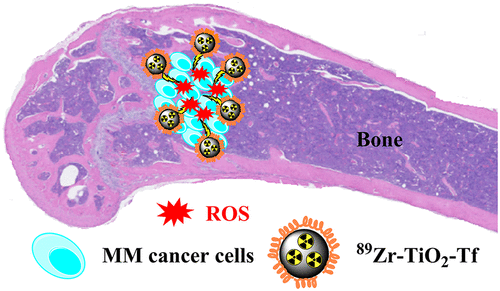
Rui Tang, et al. Osteotropic Radiolabeled Nanophotosensitizer for Imaging and Treating Multiple Myeloma, ACS Nano, 2020.
DOI: 10.1021/acsnano.9b09618
https://doi.org/10.1021/acsnano.9b09618


















