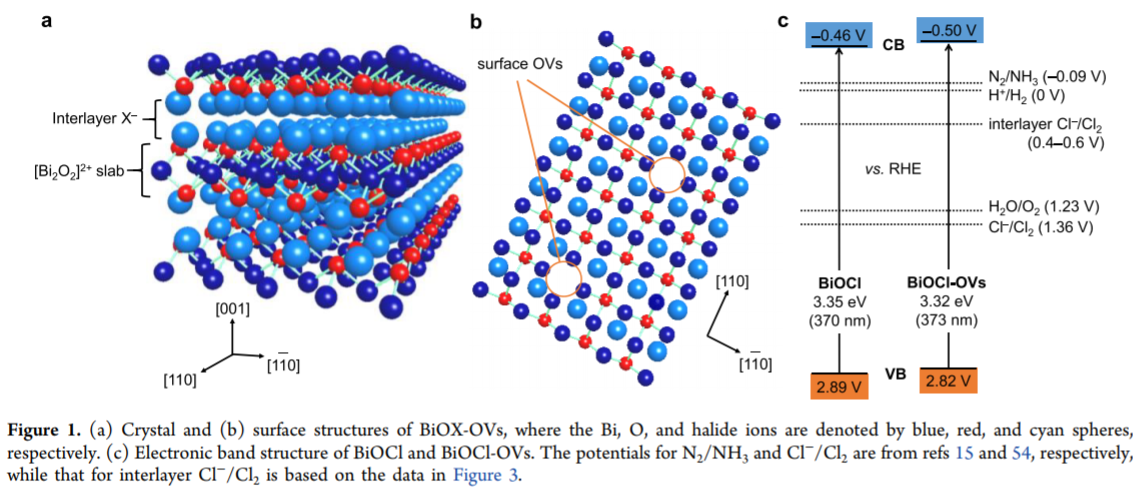
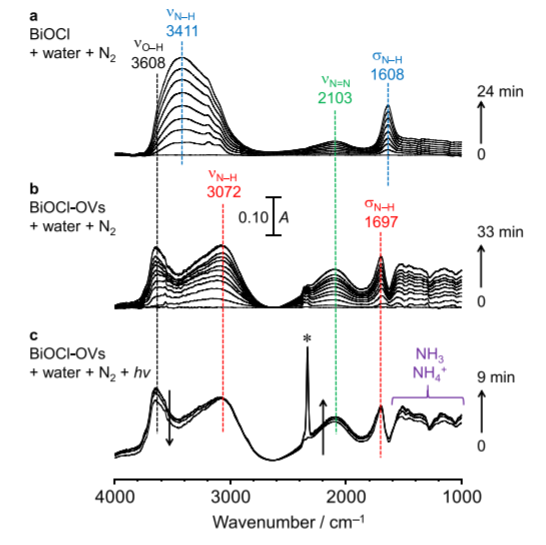
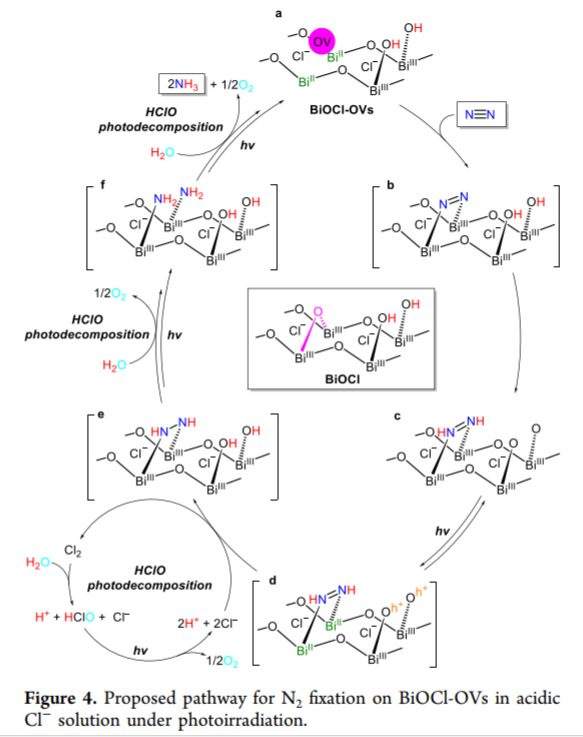
NH3是重要的化学品,通过光催化N2还原是个比较好的选择方案,之前的报道中这种光催化还原过程的速率较低。日本大阪大学的Yasuhiro Shiraishi、关西大学等报道了一种界面氧空穴BiOCl材料在光催化N2还原中的应用,该方法中使用紫外光作为光源,使用含有Cl-的水溶液,N2气流经过溶液并实现了高效率还原。界面上的氧空穴物种氧化溶液中的Cl-,并生成HClO。生成的HClO在紫外光作用中实现了分解为O2和Cl-。该过程中通过氧化H2O,生成NH3。该过程中溶液中的KCl中的Cl-能够使催化剂界面上反应的Cl-恢复。
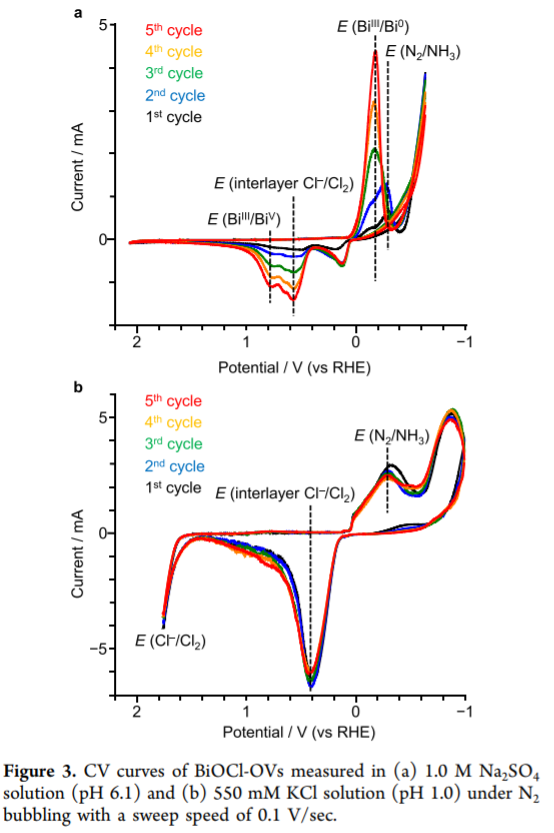
该反应在不加入Cl-的纯水中失活。测试了催化剂的电化学性质,测试了1 M Na2SO4 pH 6.1,550 mM KCl pH 1在N2气氛中的循环氧化还原性能。进行了5次循环测试,首次测试循环过程未出现水氧化阳极电流,有N2还原对应的电流(-0.3 V),随后的测试过程中发现,N2还原过程被抑制了。
参考文献
Yasuhiro Shiraishi*; Masaki Hashimoto; Kiyomichi Chishiro; Kenta Moriyama; Shunsuke Tanaka; Takayuki Hirai
Photocatalytic Dinitrogen Fixation with Water on Bismuth Oxychloride in Chloride Solutions for Solar-to-Chemical Energy Conversion
J Am Chem Soc 2020, DOI: 10.1021/jacs.0c01683
https://pubs.acs.org/doi/abs/10.1021/jacs.0c01683