
FOLFOX是亚叶酸(FnA),5-氟尿嘧啶(5-Fu)和奥沙利铂(OxP)的组合策略,几十年来一直用作大肠癌(CRC)的标准治疗方法。尽管患者的存活率提高了,但是仍然具有功效低、毒性高和疗程长等诸多缺点。因此,需要开发出新的策略来解决这些问题,方便进一步的临床应用。
为此,美国北卡罗来纳大学教堂山分校黄力夫教授团队使用纳米沉淀技术在油包水反向微乳液中开发了AEAA靶向的PEG化脂质纳米颗粒(即Nano-Folox),该Nano-Folox和5-Fu的组合有效地在原位CRC小鼠中实现了化学免疫治疗。
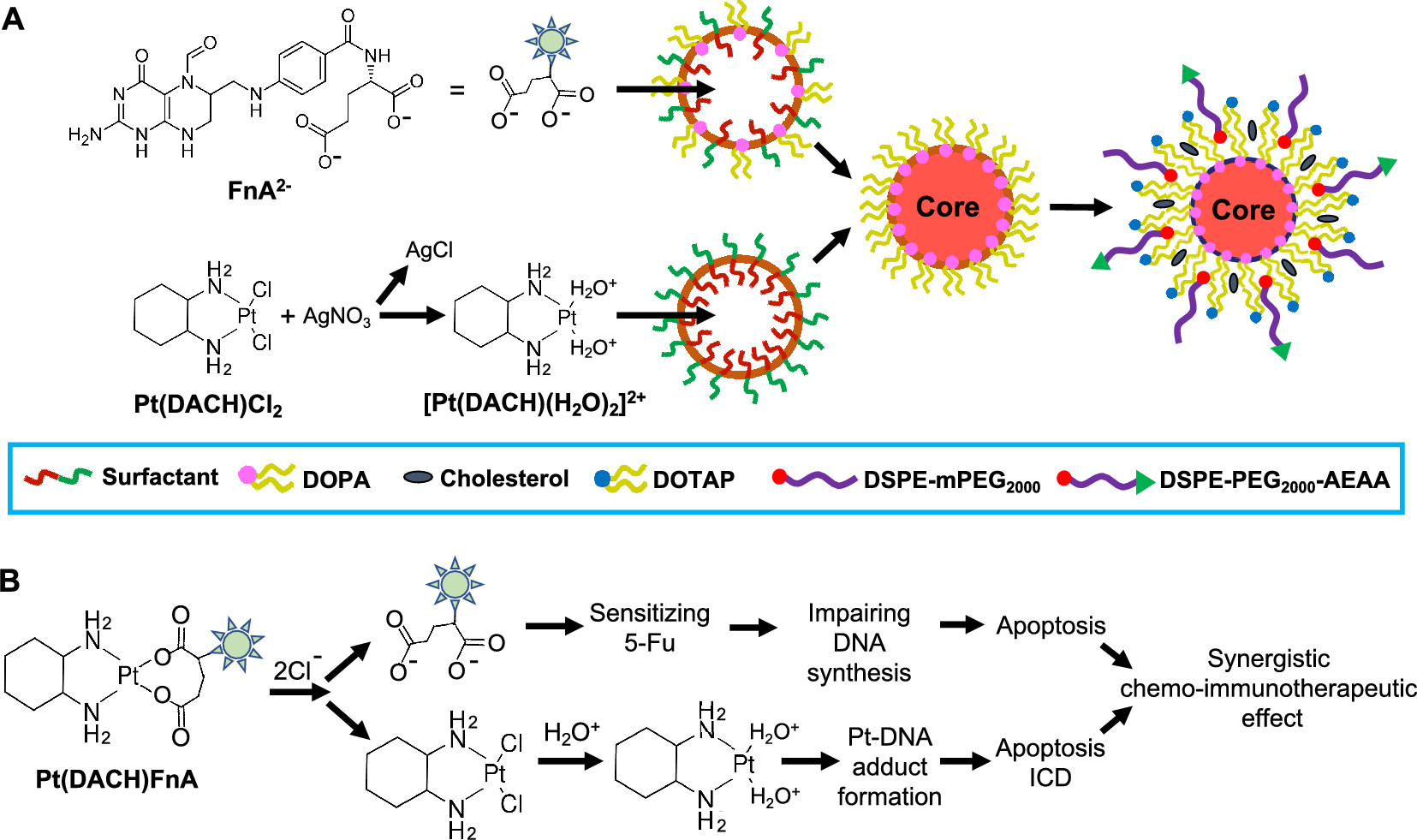
图 | 使用纳米沉淀技术在微乳液中配制的Nano-Folox示意图。
本文要点
1)研究人员通过活性形式的OxP([Pt(DACH)(H2O)2]2+)和FnA形成纳米沉淀物(C26H35N9O7Pt),然后使用纳米沉淀技术将其配制为微乳液中AEAA靶向的PEG化脂质纳米颗粒(即Nano-Folox),实现了OxP衍生物和FnA的共递送。在原位CRC小鼠模型中, Nano-Folox显著促进了铂药物和FnA的血液循环和肿瘤蓄积。新兴证据表明,OxP不仅可以提供抗癌毒性作用,还可以诱导免疫原性细胞死亡。因此,Nano-Folox在原位CRC小鼠中表现出良好的化学免疫治疗活性。
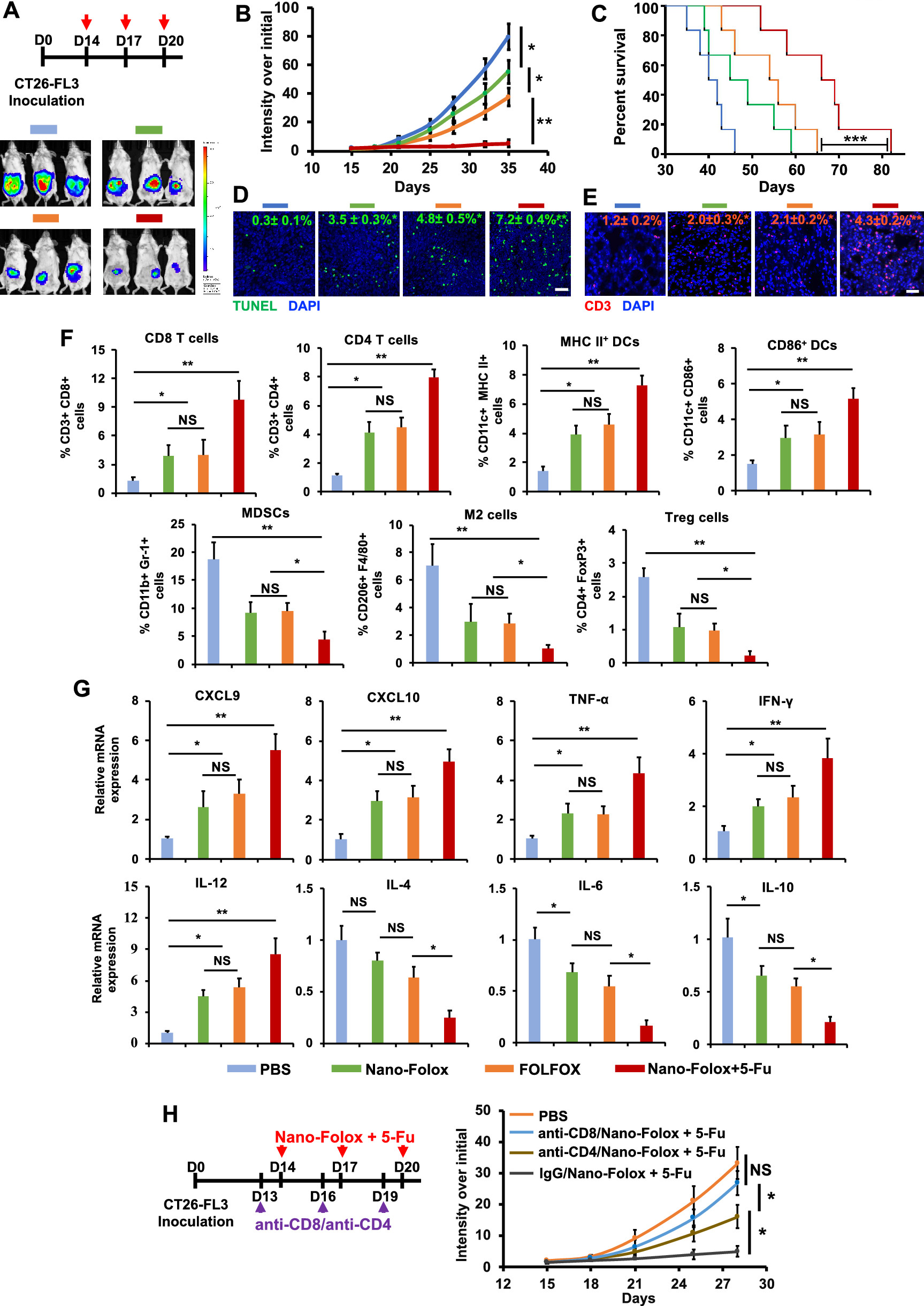
图 | Nano-Folox和Nano-Folox/5-Fu对原位大肠癌小鼠的化学-免疫治疗作用。
2)同时,5-Fu用作游离药物可以促进Nano-Folox的治疗功效。这种化学疗法和免疫疗法的组合有望获得比单药疗法更好的抗癌效果,而且没有显示出毒性。更重要的是,anti-PD-L1 mAb增强了Nano-Folox / 5-Fu体系,进一步延缓了小鼠肝转移的速度。
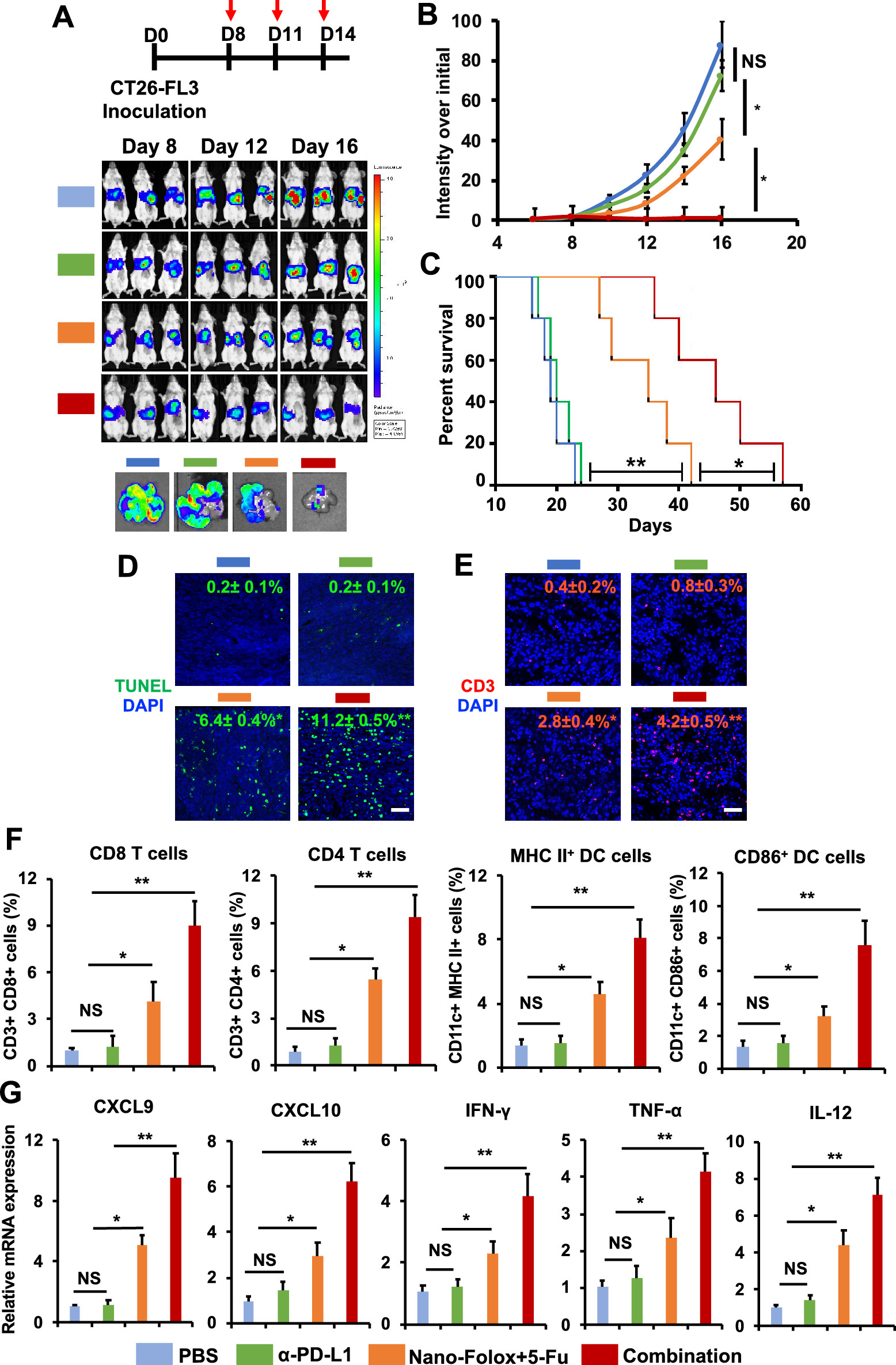
图 | Nano-Folox/5-Fu和anti-PD-L1联合用于肝转移小鼠的化学-免疫治疗
3)这种联合治疗的抗癌机制可能是:a. Nano-Folox中从Pt(DACH)·FnA释放的FnA促进了5-Fu的效力,而5-Fu / FnA又增加了OxP衍生物的效力;b. Nano-Folox / 5-Fu诱导免疫原性细胞死亡,从而重新编辑免疫抑制肿瘤微环境,使“冷”肿瘤变成“热”肿瘤,并用anti-PD-L1 mAb增强免疫治疗效果。
总而言之,就药物载量和活性形式的OxP和FnA的肿瘤蓄积而言,Nano-Folox作为基于纳米颗粒的形式颇具前途,与已报道的基于OxP的纳米颗粒和传统的FOLFOX相比具有明显优势。此外,Nano-Folox/5-Fu策略与免疫检查点抑制剂联合使用,对初级和转移阶段的大肠癌患者具有更高的化学-免疫双重疗效。
参考文献:
Jianfeng Guo et al. Nano Codelivery of Oxaliplatin and Folinic Acid Achieves Synergistic Chemo-Immunotherapy with 5-Fluorouracil for Colorectal Cancer and Liver Metastasis. ACS Nano. 2020.
https://doi.org/10.1021/acsnano.0c01676



















