
超分子纳米材料作为药物载体,具有高稳定性、强大的包容能力和易被修饰等优点,近来受到广泛的关注。然而,具有长期血液循环,高效肿瘤细胞摄取和在肿瘤细胞内部定向释放药物等综合能力的智能药物仍然相当有限。近日,南开大学丁丹、浙江大学金桥等教授报道了一种使用超分子聚集诱导发光(AIE)的纳米点进行成像指导的药物递送策略,整合了AIE和超分子纳米材料的优点,具有增强的癌细胞摄取、可控的药物释放和良好的肿瘤抑制能力。浙江大学计剑教授为文章的共同作者。
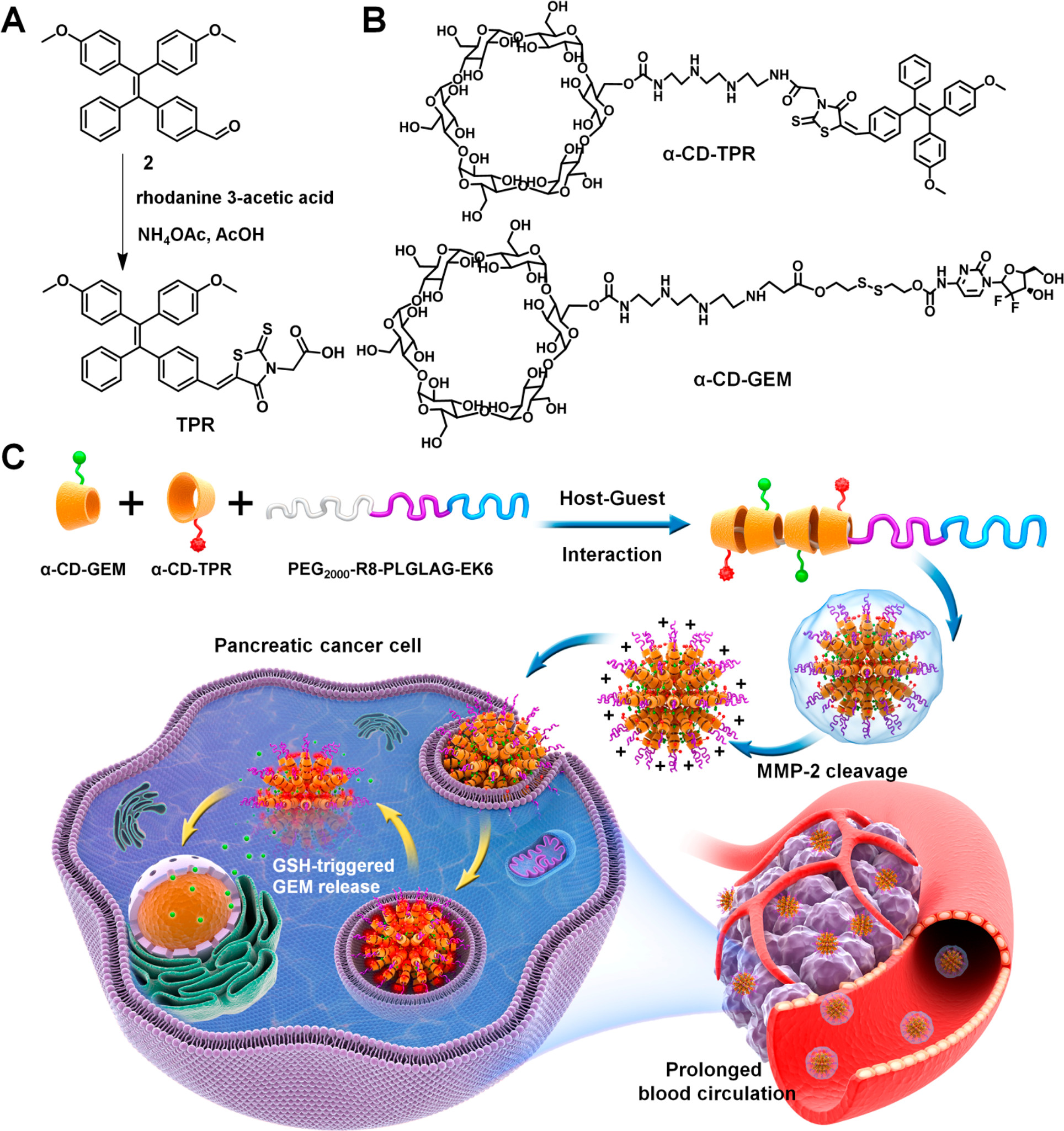
图 | 制备过程和作用示意图。
本文要点
1)研究人员通过利用对基质金属蛋白酶-2(MMP-2)敏感的PEG肽和功能性α-环糊精(α-CD)衍生物(与抗癌药GEM和基于远红/近红外AIE荧光分子结合)的主客体相互作用,开发了一种超分子AIE点,作为GEM药物的纳米载体。
2)超分子AIE点凭借两性离子隐形肽EK6,实现长时间的血液循环。通过增强的通透性和保留效应,在肿瘤组织中大量积累后,超分子AIE点可以连续响应肿瘤过表达的MMP-2和细胞内还原性微环境,从而增强癌细胞的摄取和癌细胞内选择性GEM释放。皮下和原位胰腺癌肿瘤模型的实验结果均显示出优异的肿瘤抑制能力。
3)与目前可用的纳米热学体系相比,这项研究的重要性包括:a. 提出一种超分子AIE点的概念,融合了超分子纳米材料和AIE荧光分子在成像指导的药物输送和癌症治疗上的优势; b. 这是极少数的、可以同时实现延长的血液循环和程序化的肿瘤微环境反应性的智能超分子药物纳米载体; c. 尽管已经开发了用于体内胰腺癌治疗的大量药物纳米载体,但是据报道有限的药物纳米载体对原位胰腺肿瘤有效。
总之,该研究工作提出新型超分子AIE点的概念,融合了超分子纳米材料和AIE荧光分子在成像指导的药物输送和癌症治疗的优势。这个成功的例子表明超分子纳米平台有望用于开发先进的药物递送系统。
参考文献:
Xiaohui Chen et al. Supramolecular Aggregation-Induced Emission Nanodots with Programmed Tumor Microenvironment Responsiveness for Image-Guided Orthotopic Pancreatic Cancer Therapy. ACS Nano. 2020.
https://doi.org/10.1021/acsnano.0c02197



















