基因改造免疫细胞的过继转移对于癌症免疫疗法具有广阔的前景。CRISPR敲入靶向可以改善细胞疗法,但需要更多的高通量方法来测试哪种敲入基因载体能够最有效地增强体内原代细胞的功能。有鉴于此,美国加州大学旧金山分校Alexander Marson、Theodore L. Roth等研究人员,开发了用于细胞免疫疗法基因组改造的集合敲入技术。
本文要点
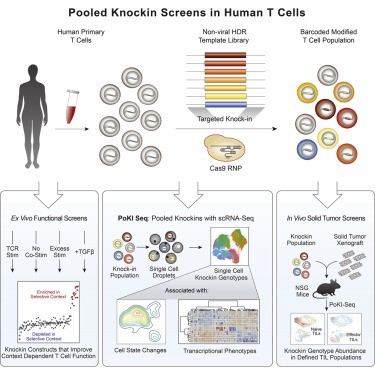
1)研究人员开发了一种广泛适用的技术来条形编码和追踪大型非病毒DNA模板的靶向整合,并将其应用于在原代人T细胞中进行集合敲入筛选。
2)通过将数十种独特条形码模板的集合敲入到T细胞受体(TCR)-基因座中,研究人员揭示了可增强体外和体内适应性的基因载体。
3)研究人员进一步开发了集合敲入测序(PoKI-seq)技术,其结合了单细胞转录组分析和集合敲入筛选,从而能够测量体外和体内的细胞丰度和细胞状态。
4)该平台发现了一种新型的转化生长因子β(TGF-β)R2-41BB嵌合受体,可改善实体瘤清除率。
集合敲入筛选实现了内源基因序列的并行重写,从而能够加快细胞疗法的发现。
参考文献:
Theodore L. Roth, et al. Pooled Knockin Targeting for Genome Engineering of Cellular Immunotherapies. Cell, 2020.
DOI:10.1016/j.cell.2020.03.039
https://www.cell.com/cell/fulltext/S0092-8674(20)30332-9


















