高效的放疗增敏剂一般都具备两个重要特征:一是可以选择性地靶向肿瘤细胞,通过诱导致死DNA损伤以提高治疗效果;二是能够被快速清除,以实现良好的生物相容性。山东大学夏海兵教授、浙江大学毛峥伟教授和王伟林教授制备了一种直径小于5nm的超小金纳米颗粒(Au NPs),并在其表面包覆了一种多功能肽,使其具有被肿瘤细胞选择性摄取的能力。
本文要点:
(1)实验将一种由三种构建块组成的响应型肽(Tat- r - ek)对超小的金纳米粒子进行包覆修饰,并利用透射电子显微镜和动态激光散射研究了Au@Tat-R-EK纳米材料的形貌、胶体稳定性和响应性;通过ICP-MS研究了Au@Tat-R-EK NPs在肿瘤组织中的选择性摄取和积累效果,并就Au@Tat-R-EK NPs对HepG2癌细胞的细胞毒性进行了评估;最后在体内验证了该材料对原位LM3肝癌的肿瘤杀伤能力。
(2)实验结果表明,该多功能多肽修饰的超小Au NPs具有很好的胶体稳定性和对组织蛋白酶b响应的表面变化,使得其可以在体外被癌细胞选择性摄取并在体内积累到肿瘤部位。在x射线照射下,该响应型Au NPs在体外具有良好的放疗增敏细胞毒性,而在体内对小鼠肝癌也有较好的治疗效果。并且由于其超小的尺寸,该粒子也可以快速地从体内被清除,使其在将来的临床应用中也具有很好的体内生物相容性。
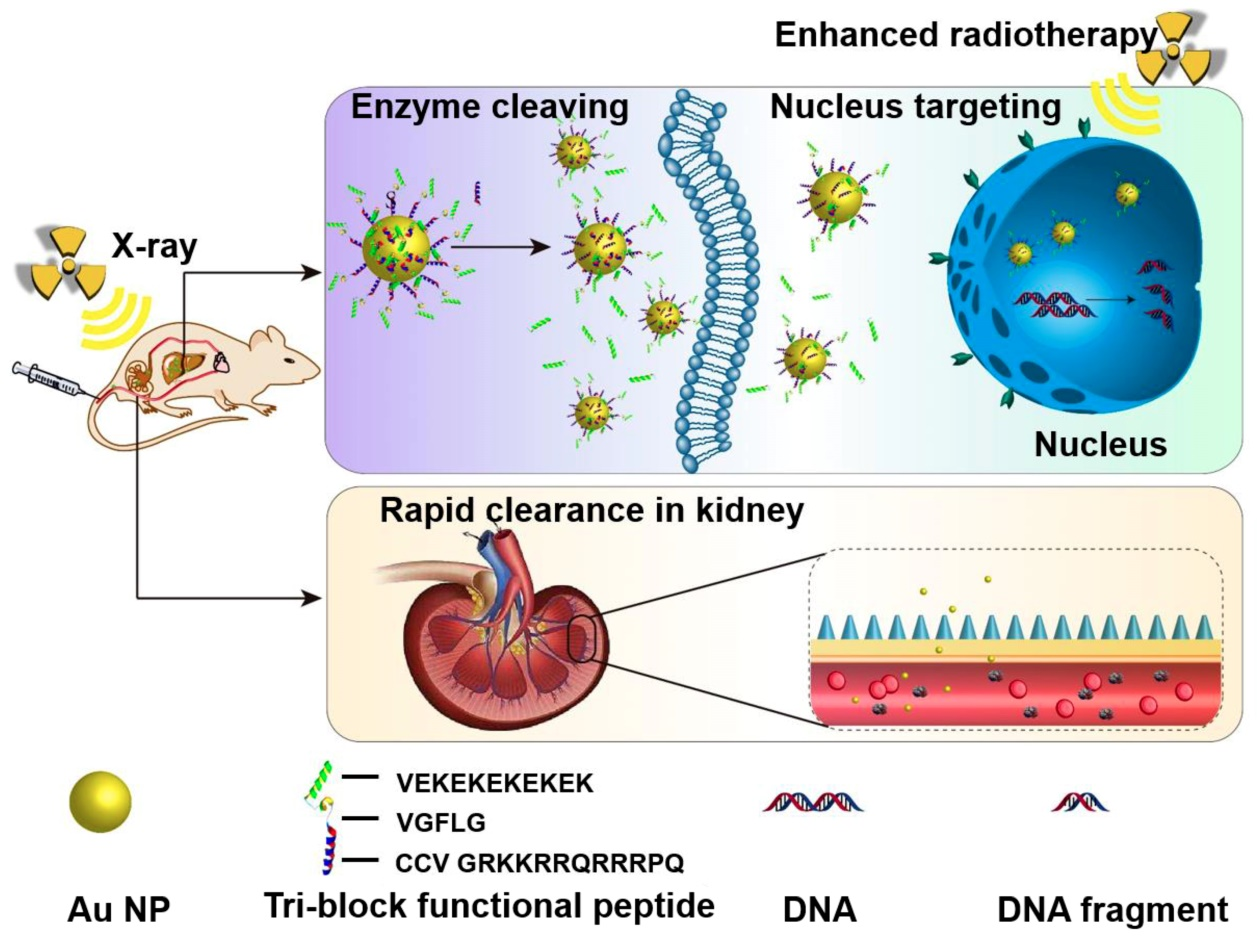
Yuan Ding. et al. Tumor microenvironment-responsive multifunctional peptide coated ultrasmall gold nanoparticles and their application in cancer radiotherapy. Theranostics. 2020
DOI: 10.7150/thno.45017
https://www.thno.org/v10p5195.htm



















