活性氧(ROS)耗竭和低ROS产生分别是由于肿瘤内氧化还原代谢平衡和从超声机械能到ROS代表的化学能的低能量转换效率,是声动力治疗(SDT)的两个重要抑制因素。为了解决这两个问题,同济大学Kun Zhang、Hui‐Xiong Xu、Chang Liu等人构建了一个肿瘤代谢工程化复合纳米平台,能够干预肿瘤内的ROS代谢,打破氧化还原平衡,重塑肿瘤微环境,以增强SDT的抗肿瘤作用。
本文要点:
1)在这个代谢工程化纳米平台中,Nb2C纳米片作为支架来容纳TiO2声敏剂和丁硫氨酸-亚砜亚胺。
2)系统的实验表明,这种纳米平台可以通过抑制谷胱甘肽的合成,同时通过Nb2C增强电子-空穴对的产生和分离来促进ROS的产生,从而减少ROS的消耗。
3)在联合作用下,净ROS含量可显著提高,从而在体内和体外产生高效的抗肿瘤效果。此外,这种结合的设计原则,即调节肿瘤代谢以减少ROS消耗和电子-空穴对分离以促进ROS的产生,可以推广到其他依赖ROS的治疗系统。
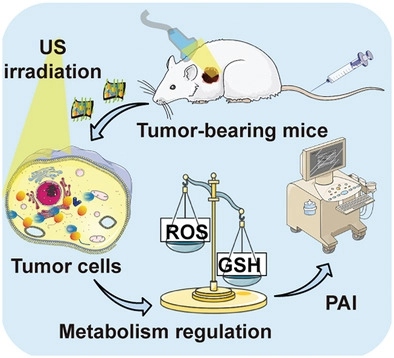
Xin Guan, et al. Tumor Metabolism‐Engineered Composite Nanoplatforms Potentiate Sonodynamic Therapy via Reshaping Tumor Microenvironment and Facilitating Electron–Hole Pairs’ Separation, Adv. Funct. Mater. 2020.
DOI: 10.1002/adfm.202000326
https://doi.org/10.1002/adfm.202000326


















