脂肪一级胺在天然产物、药品、功能材料中大量存在,尽管目前存在大量的合成方法,通过活化C(sp3)-H键将胺基引入的方法很少,加州理工学院Frances H. Arnold等发现通过酶催化能够直接活化C(sp3)-H键构建胺基,并且展现了较高的化学选择性、区域选择性、对映选择性。该方法中通过羟胺衍生物作为胺源,通过对P411酶进行基因编辑(用Ser配体修饰,将连接在血红素铁上的Cys配体替换),实现了对多种官能团修饰的苄基C-H、脂肪族分子中烯丙基C-H键上进行官能团化,转化为手性胺基。这种生物酶催化反应效率较高(TTN达到3930),对映选择性较高(达到96 % ee)。
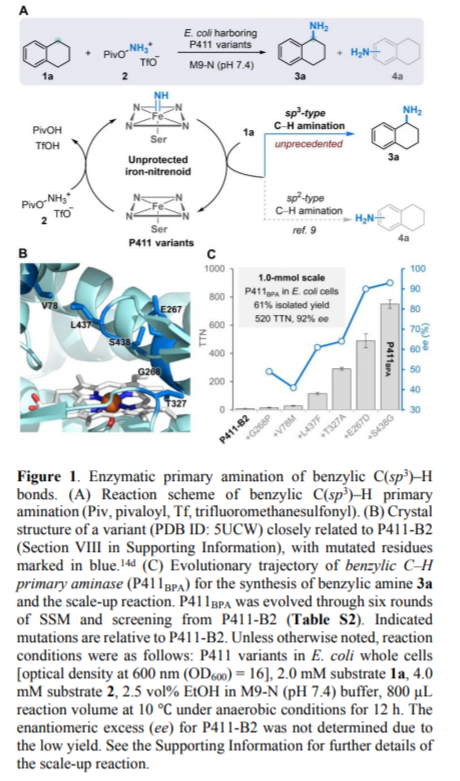
反应优化。羟胺的酯化物(PivO-NH3+OTf-)作为胺源,在无氧环境中抑制O2对反应的影响,在大肠杆菌(Escherichia coli)细胞中的酶作为催化剂,pH 7.4的M9-N中于10 ℃中反应。
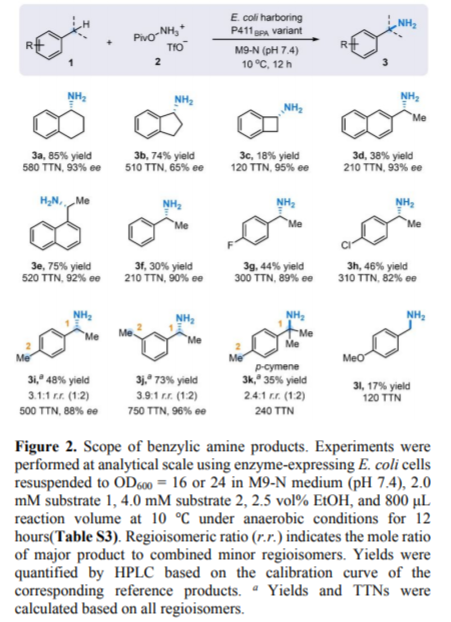
通过胺基酶(primary amineases)催化,对一级、二级、三级苄基碳上的C-H键/脂肪烃分子中的烯丙基C-H键进行了有效的胺基化,体现了较高的反应位点选择性、对映选择性。
参考文献
Zhi-Jun Jia, Shilong Gao, and Frances H. Arnold*
Enzymatic Primary Amination of Benzylic and Allylic C(sp3)–H Bonds,J. Am. Chem. Soc. 2020
DOI:10.1021/jacs.0c03428
https://pubs.acs.org/doi/10.1021/jacs.0c03428


















