含有基因药物的脂质纳米颗粒(lipid nanoparticle)通过生物编辑方法实现了生物分布的调控,并引发了器官特异性基因调控(organ-specific gene regulation)。
埃因霍温科技大学Roy van der Meel对最近含有基因药物的脂质纳米颗粒的发展在Nature Nanotechnology上进行总结和评述。脂质纳米颗粒(lipid nanoparticle)被应用于临床转译(clinical translation),并被美国食品药品监督管理局FDA认证了应用于siRNA干扰素药物,这种纳米药物用于治疗遗传性疾病甲状腺素介导的疾病引发的多发性神经病(polyneuropathies),该过程通过静脉输液脂质纳米颗粒/siRNA传输到肝细胞,抑制了病理蛋白生产过程。脂质纳米颗粒同时能将信使RNA(mRNA)组装,进而引发治疗性蛋白的生产,并通过基因编辑方法改善疾病引发的肝细胞突变。但是在肝以外的组织和器官中的应用仍没有相关报道。
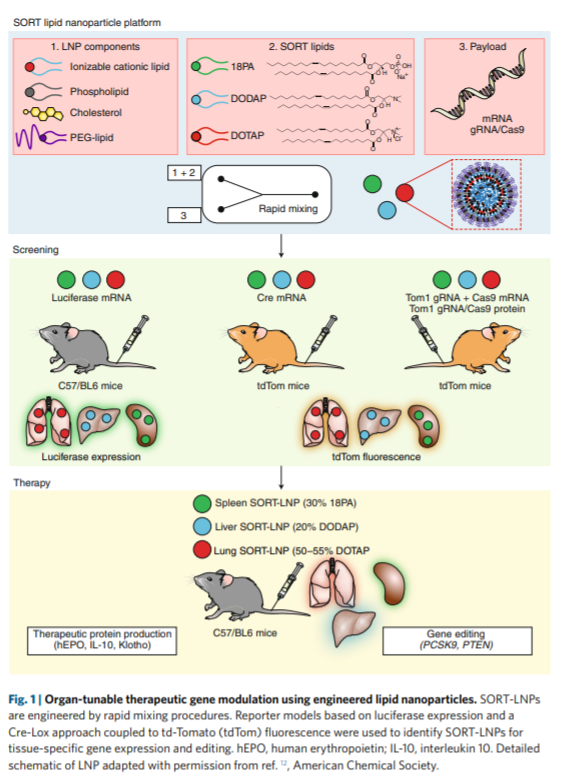
美国德克萨斯大学西南医学中心Daniel J. Siegwart等在Nature Nanotechnology上报道了一种选择性器官靶点(selective organ targeting, SORT)方法,其中含有核酸的脂质纳米颗粒能够对肾脏、脾、肺的基因进行调控。脂质纳米颗粒含有磷脂,胆固醇,聚乙二醇和离子化的阳离子脂质。脂质纳米颗粒中的组分通过优化后能够将核酸传输到肝细胞中。在SORT中,作者在磷脂,胆固醇,聚乙二醇和离子化的阳离子脂质外,加入第五种组分用来传输信使RNA并对老鼠中特定的组织进行基因编辑。通过快速的混合,对SORT脂质的各部分的组成和含量进行了系统的调控,通过对SORT中加入不同量的阳离子型1,2-二油酰-3-三甲基丙烷基氯化铵(DOTAP),荧光素酶表达能从肝转移到脾、肾上(0%DOTAP为最佳肝脏转染,10-15%适合脾脏转染,而50%为最佳肺部转染)。当含有10~40 %的阳离子脂质1,2-二油酰-sn-甘油-3-磷酸(1,2-dioleoyl-sn-glycero-3- phosphate,18PA),实现了对脾以外的部分进行表达。加入20 %的DODAP,对生物分布过程没有影响,但是提高了信使RNA向肾的传输过程。SiRNA药物Onpattro的荧光素酶表达同样能够进行调控。此外,作者还报道了其在CRISPR/Cas基因编辑中的作用,在内源性靶基因(PTEN)和治疗靶基因(PCSK9)中的作用。
本文的创新性在于,对多达数百种脂质纳米颗粒的大规模筛选,并鉴定其在传输功能性的信使RNA作用。
参考文献
1. Roy van der Meel*
Nanotechnology for organ-tunable gene editing,Nat. Nanotechnol. 2020, 15, 253-255
DOI:10.1038/s41565-020-0666-9
https://www.nature.com/articles/s41565-020-0666-9
2. Qiang Cheng, Tuo Wei, Lukas Farbiak, Lindsay T. Johnson, Sean A. Dilliard & Daniel J. Siegwart*
Selective organ targeting (SORT) nanoparticles for tissue-specific mRNA delivery and CRISPR–Cas gene editing,Nat Nanotechnol 2020, 15, 313-320
DOI:10.1038/s41565-020-0669-6
https://www.nature.com/articles/s41565-020-0669-6


















