化学蛋白质合成可以在蛋白质骨架的精确位置上系统整合一种或多种非天然氨基酸,从而可以进行结构功能关系研究。但是,固相肽合成(SPPS)通常限于50个残基的肽,因此,化学蛋白质合成需要天然的化学连接(NCL)反应来实现未受保护肽片段在溶液中的化学选择性偶联。这种组合的多步骤方法通常需要至少三个肽片段的合成和顺序连接才能获得蛋白质,这一过程仍然比较费力。
有鉴于此,麻省理工学院B. L. Pentelute等人报道了一种高效的化学反应,与一种自动快速流动仪器相匹配,用于直接制造长达327个连续反应的164个氨基酸的肽链。这台机器很快:肽链的延伸在几小时内就完成了。
本文要点:
1)首先使用30个残基的胰高血糖素样肽1作为测试,为每种氨基酸掺入建立了特定的最佳条件集。然后,他们将优化的程序应用于9种不同蛋白质的合成,从而建立了通过自动化快速流肽合成(automated fast-flow peptide synthesis,AFPS)技术进行总化学蛋白质合成的通用方案。与通过生物表达产生的蛋白质进行的比较分析证实,在这项研究中获得的合成蛋白质表现出相似的结构和功能。
2)除了其令人印象深刻的速度外,这项新技术还使AFPS技术可达到的肽大小极限提高了三倍。这一进展将促进未来蛋白质合成的努力,并影响多个研究领域。将AFPS技术与现有的NCL方法结合使用,可以在单个连接反应后递送> 300个残基的蛋白质。
3)此外,不难想象,对各种各样的非天然氨基酸残基进行了类似的优化工作,将其效用范围扩展到目前的范围之外,并可能产生生物方法无法获得的全非天然蛋白质模拟材料。在这方面,它不仅会赶上核糖体能力,而且会超越核糖体能力。
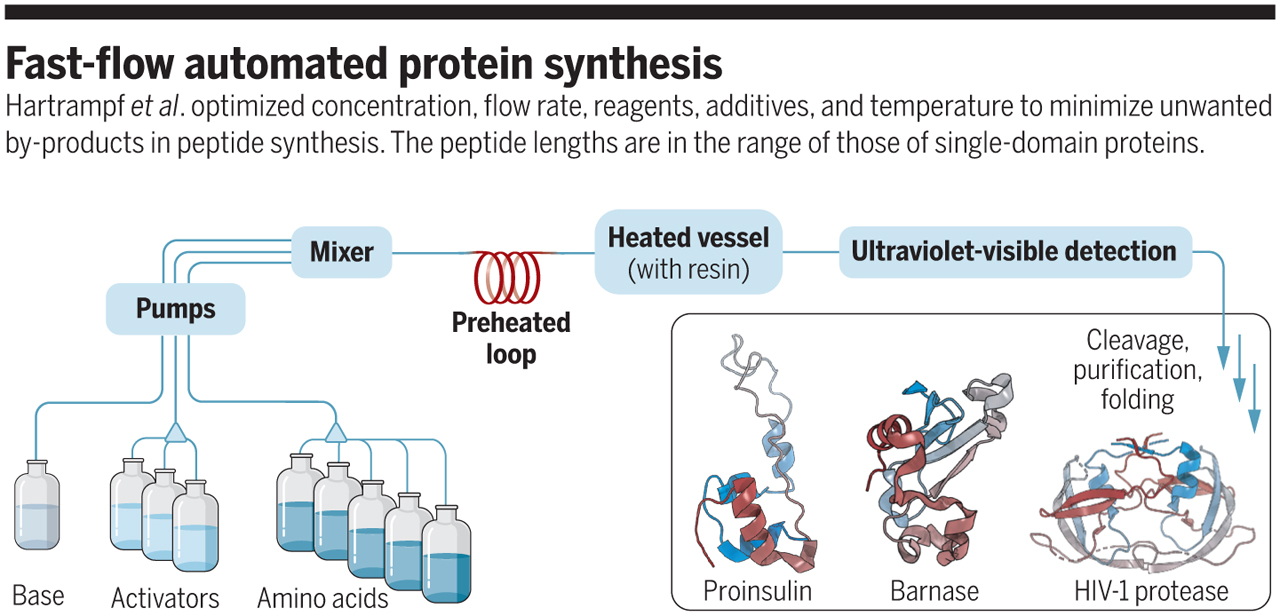
N. Hartrampf et al., Synthesis of proteins by automated flow chemistry. Science 368, 980 (2020).
DOI: 10.1126/science.abb2491
https://doi.org/10.1126/science.abb2491


















