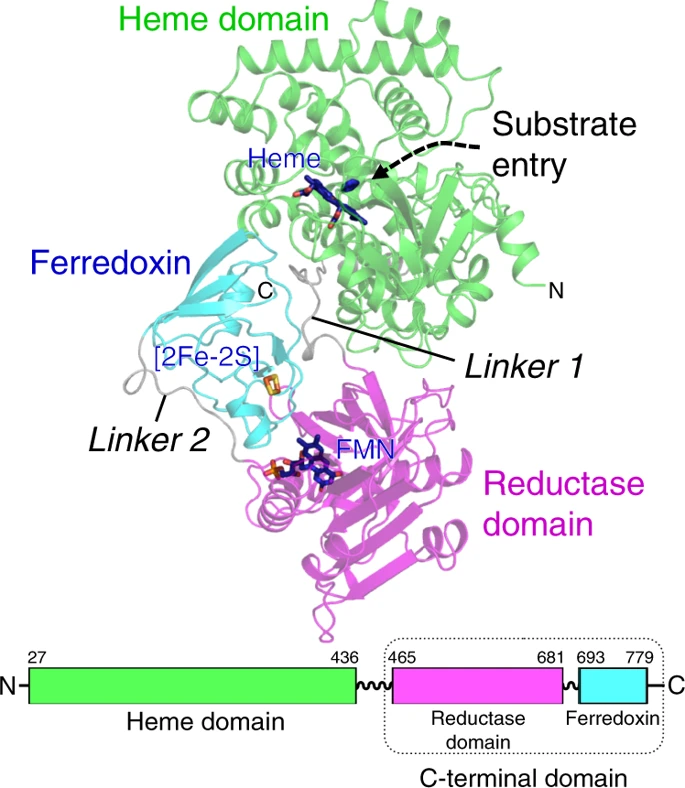
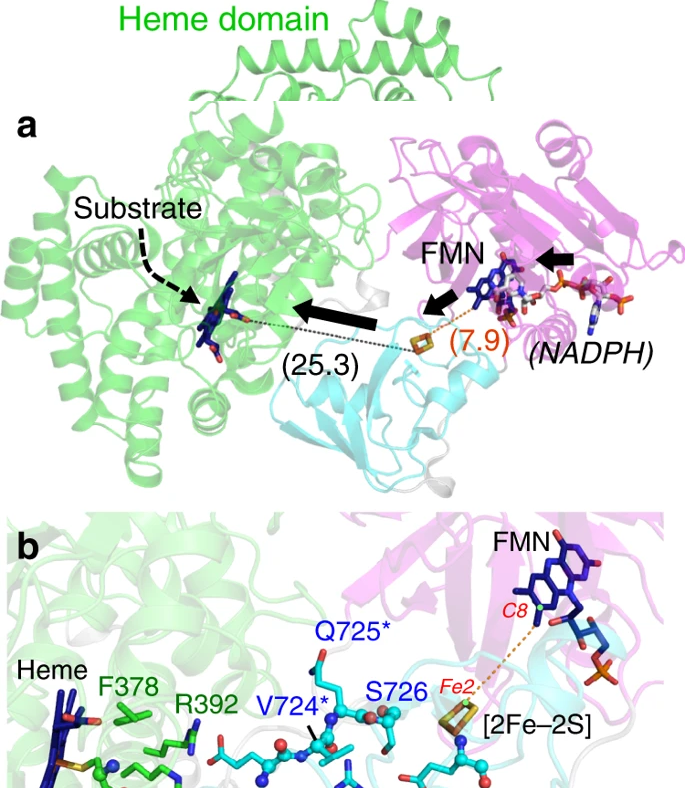
P450单加氧酶(Cytochrome P450 monooxygenases)是一种含硫醇的血红素酶,并且对多种反应有催化作用。P450单加氧酶中在单个多肽链中含有还原配合物。湖北大学陈纯琪、郭瑞庭等展示了P450中的CYP116B46整体晶体结构,结果显示多肽链中含有三个主要功能区域,实现了电子从FMN通过[2Fe-2S]簇传输到血红素中,并且[2Fe-2S]和FMN之间的距离非常近,有效的进行高效电子传输。结果显示,[2Fe-2S]和血红素之间的距离为2.53 nm。结果显示在[2Fe-2S]和血红素之间存在多个残基,并在催化反应中起到作用。这些发现为理解P450中的分子间电子传输过程有帮助,同时为开发P450的生物技术应用提供了丰富经验。
蛋白结晶方法。在25 ℃中进行晶体的结晶,通过沉滴蒸气扩散法(sitting-drop vapor-diffusion method)进行。将1 μL蛋白和1 μL溶液在96孔板上进行混合结晶。在4天后通过PEGRxTM screen 47获得了最初的CYP116B46结晶,随后优化结晶环境得到高质量的晶体。
参考文献
Lilan Zhang, Zhenzhen Xie, Ziwei Liu, Shuyu Zhou, Lixin Ma, Weidong Liu, Jian-Wen Huang, Tzu-Ping Ko, Xiuqin Li, Yuechan Hu, Jian Min, Xuejing Yu, Rey-Ting Guo* & Chun-Chi Chen*
Structural insight into the electron transfer pathway of a self-sufficient P450 monooxygenase, Nature Commun. 2020, 11, 2676
DOI:10.1038/s41467-020-16500-5
https://www.nature.com/articles/s41467-020-16500-5


















