纳米药物的抗癌作用很大程度上受到肿瘤内渗透性不足的阻碍。在此,苏州大学刘勇、殷黎晨等人设计了一种改善肿瘤微环境(TME)的和自适应的纳米团簇(NCs)能够耗尽肿瘤相关成纤维细胞(CAFs)和转换大小/电荷,以介导光辅助的分级的肿瘤内穿透。
本文要点:
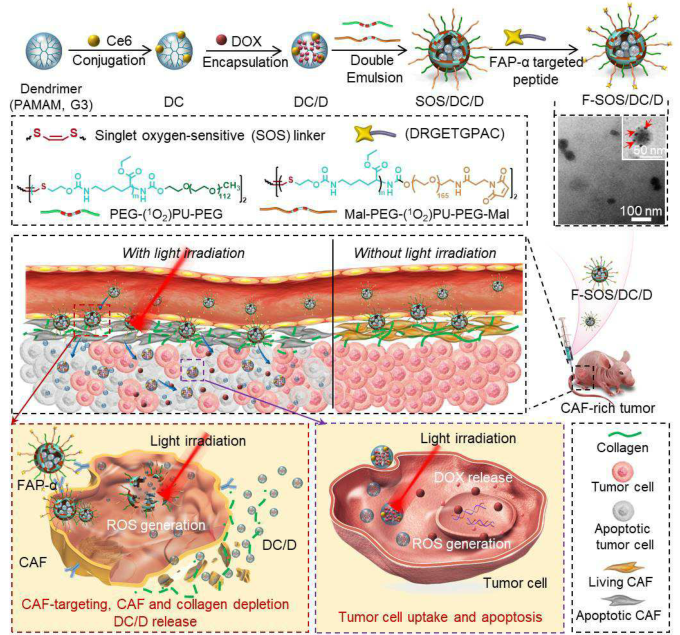
1)通过FAP-α靶向肽修饰的1O2敏感聚合物的自组装,制备了大尺寸(~50 nm)的NCs,并进一步将其用于包裹与Ce6偶联并负载DOX(DC/D)的小尺寸树枝状大分子(~5 nm)。
2)全身给药后,NCs有效地靶向CAFs,并在光照射下产生致死水平的1O2,这耗尽了CAFs,并伴随着NCs的解离,从而释放出小尺寸的带正电荷的DC/D。
3)这种间质衰减和NCs转化共同促进了DC/D向富含CAF的肿瘤的深层区域输送,在那里DOX和1O2产生了协同抗癌效果。
本研究为促进纳米药物在肿瘤中的渗透提供了一种有效的途径,可以同时在时空上重构纳米药物的性质,重塑TME。
Jing Yan, et al. Light-Assisted Hierarchical Intratumoral Penetration and Programmed Antitumor Therapy Based on Tumor Microenvironment (TME)-Amendatory and Self-Adaptive Polymeric Nanoclusters, Biomaterials, 2020.
https://doi.org/10.1016/j.biomaterials.2020.120166


















