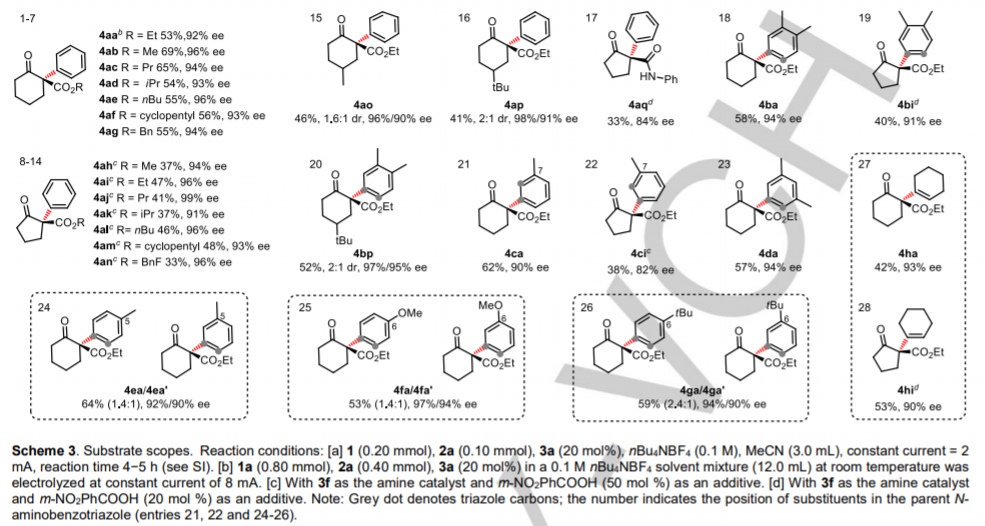
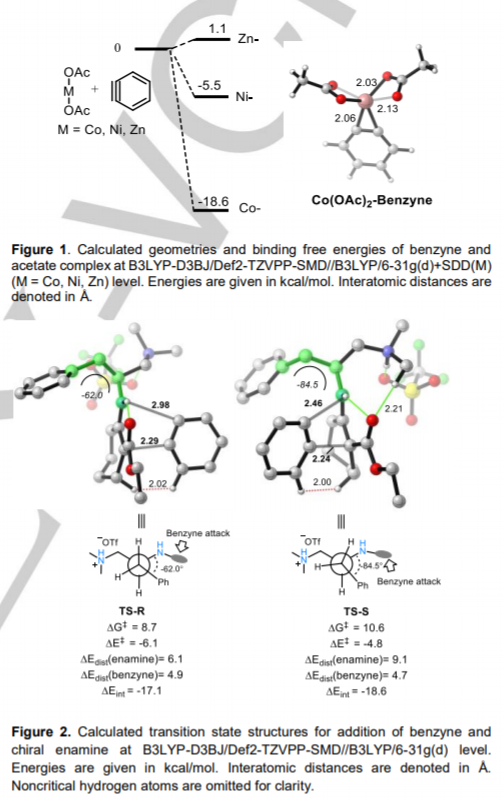
苯炔的不对称合成反应具有较高难度,这是由于苯炔中间体寿命较短、且苯炔分子是一种非极性分子,清华大学罗三中等通过电化学方法原位生成环己炔和苯炔,并和手性一级氨基酸催化剂配合,实现了首例烯胺和苯炔(环己炔)之间的偶联反应,对苯炔实现了手性不对称合成反应。作者发现该反应中醋酸钴稳定了原位生成的苯炔,并促进了炔和烯胺的偶联反应。本文中的烯胺-苯炔偶联方法学为构建α-芳基取代/环己烯基取代的立体结构碳中心提供了新选择。
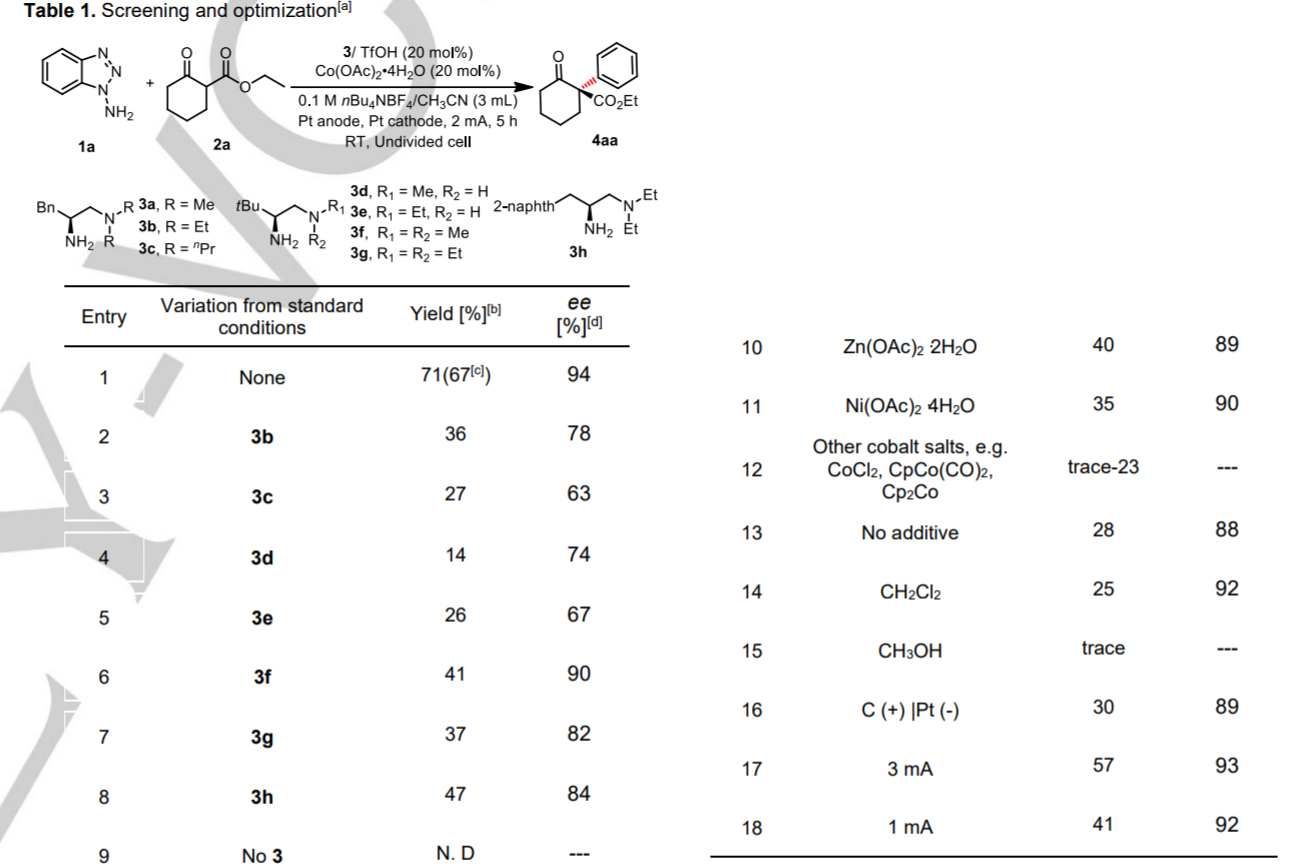
反应优化。通过2-氧代环己烷甲酸乙酯和1-氨基苯并三唑作为反应物,20 mol %的手性二胺/TfOH配体和20 mol %Co(OAc)2·2H2O作为催化剂体系,在0.1 M nBu4NBF6/CH3CN溶液中反应,以Pt作为电化学(+/-)电极,在2 mA电化学反应中于室温中反应5 h,以71 %的收率和94 % ee值进行反应。对反应物的电化学研究结果显示,1-氨基苯并三唑分子的氧化电位在0.84 V说明更容易被氧化(比手性有机胺的氧化电位更低(3a,Eox=1.54 V),同时低于烯胺中间体物种的氧化电位(Eox=1.15 V))。作者发现当反应中分别使用Zn(OAc)2·2H2O、Ni(OAc)2·2H2O,反应产率降低为40 %和35 %,同时产物的手性ee值稍微有所降低(89 %、90 %)。作者发现当反应中的正极电极更换为碳,产率降低为30 %。当反应电流更改为3 mA或1 mA,反应的产率分别降低为57 %或41 %。当反应溶剂更换为CH2Cl2或CH3OH,反应的产率分别降低为25 %和~0 %的trace量。
参考文献
Longji Li, Yao Li, Niankai Fu, Long Zhang, Sanzhong Luo*
Catalytic AsymmetricElectrochemicalα‐Arylation of Cyclic β‐Ketocarbonyls with Anodic Benzyne Intermediates, Angew. Chem. Int. Ed. 2020
DOI:10.1002/anie.202006016
https://www.onlinelibrary.wiley.com/doi/abs/10.1002/anie.202006016


















