CRISPR-Cas系统为可编程基因组编辑提供了多种工具。为了将CRISPR-Cas9介导的DNA切割的时间分辨率提高到小时时间尺度,已经做出了许多努力。于此,美国约翰·霍普金斯大学Taekjip Ha、Bin Wu和Shiva Razavi等人开发了一种caged RNA策略,该策略允许Cas9结合DNA,但在光诱导的激活作用下才能裂解。将Cas9发展成为一种精确的时间和空间控制仪器。现在应该可以实时询问细胞对DSBs的反应,这将有助于进一步了解细胞在面对这些潜在的灾难性损伤时如何保持基因组的完整性。
本文要点:
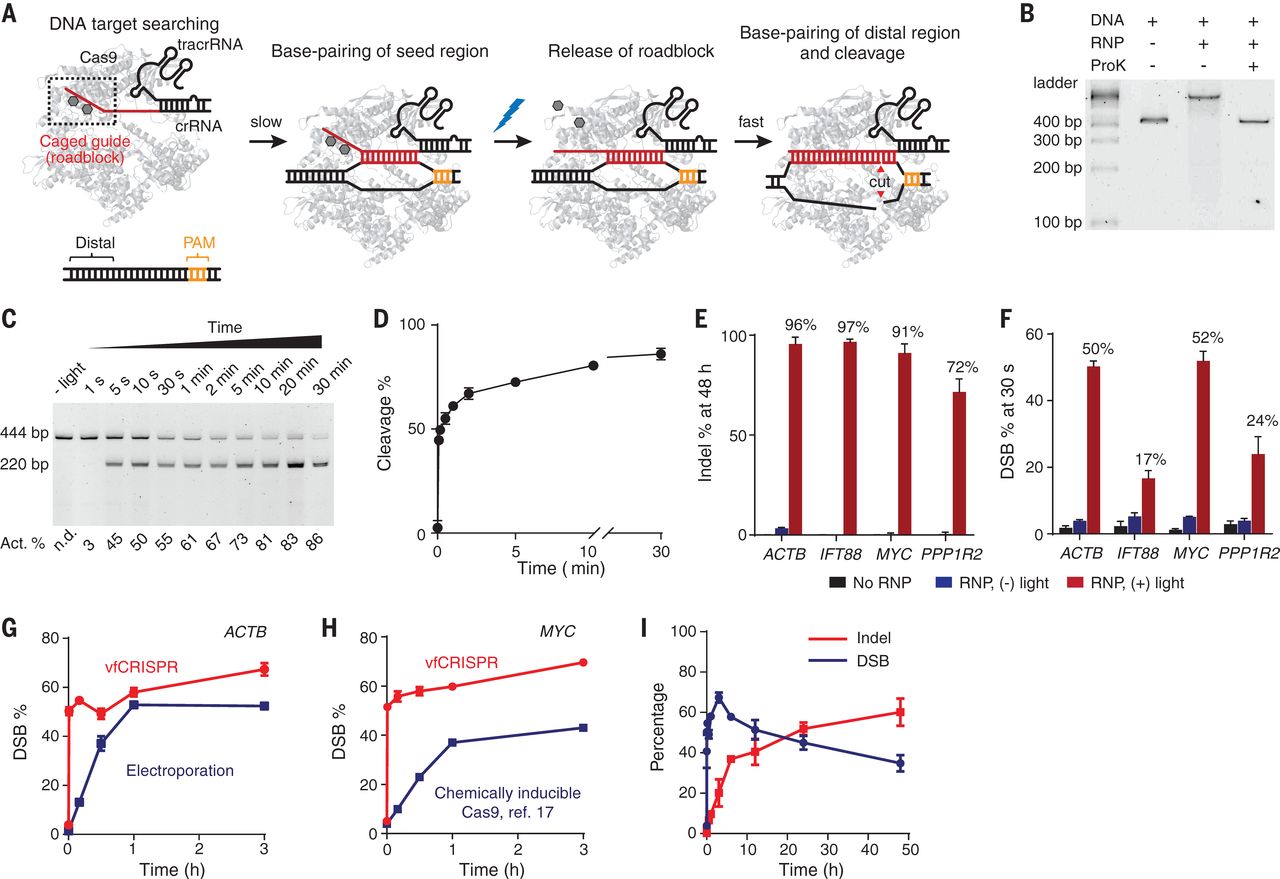
1)这种方法被称为非常快速CRISPR(vfCRISPR),在亚微米和秒尺度上产生双链断裂(DSB)。同步切割提高了DNA修复的动力学分析,显示细胞对Cas9诱导的DSBs在几分钟内反应,并且在DNA连接后可以保留MRE11。
2)DNA损伤后H2AX的磷酸化每分钟传播超过100千个碱基,达到30兆个碱基。利用单细胞荧光成像技术,研究人员研究了53BP1修复灶形成和溶解的多个周期,第一个周期比随后的周期长,并且其持续时间受修复抑制的调节。图像引导下的亚细胞Cas9激活进一步促进了单等位基因分辨率的基因组操作。vfCRISPR能够在空间、时间和基因组坐标上进行高分辨率的DNA修复研究。
Liu Y, et al. Very fast CRISPR on demand. Science. 2020;368(6496):1265-9.
DOI: 10.1126/science.aay8204
https://science.sciencemag.org/content/368/6496/1265


















