癌细胞的氧化还原状态受到活性氧(ROS)生成和消除之间的平衡的良好调节。因此,ROS水平的总体升高高于细胞耐受性阈值将导致凋亡或坏死性细胞死亡。有鉴于此,中国医学科学院北京协和医学院的Weiwei Wang、Pingsheng Huang和 天津大学的Anjie Dong等研究人员,将一种氧化应激放大剂肉桂醛(CA)与光敏剂脱镁叶绿酸A(PA)结合,通过协同的内源性和外源性途径促进ROS的产生。
本文要点
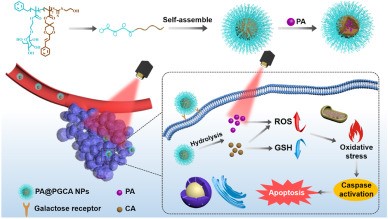
1)首先,合成了酸响应型聚半乳糖-聚肉桂醛多聚前药(简称PGCA),它可以自组装成稳定的PA纳米粒(简称PGCA@PA NPs)。
2)肿瘤细胞上半乳糖受体的丰富表达促进了PGCA@PA纳米粒的正靶向和细胞摄取效率,在此之后,由于酸性微环境下内/溶酶体隔间CA部分的脱落,PA可与PGCA纳米粒在细胞内的解离同步释放。
3)CA和PA联合光照诱导ROS水平显著升高,导致肿瘤细胞凋亡显著增加。重要的是,静脉注射PGCA@PA纳米粒能有效地抑制肝癌肿瘤的生长,不良反应可以忽略不计。
4)此外,PGCA@PA纳米粒联合抗程序性细胞死亡蛋白-1(anti-PD-1)治疗可诱导抗黑色素瘤T细胞免疫应答,并显著促进T细胞在肿瘤中的浸润。
因此,这种新颖的多前体药纳米给药系统能够通过内源性和外源性途径靶向和调控肿瘤细胞独特的氧化还原调节机制,为实现协同治疗活性和选择性提供了一条可行的途径。
参考文献:
Zujian Feng, et al. Cascade of reactive oxygen species generation by polyprodrug for combinational photodynamic therapy. Biomaterials, 2020.
DOI:10.1016/j.biomaterials.2020.120210
https://www.sciencedirect.com/science/article/pii/S0142961220304567


















