细胞内蛋白治疗的成功要求在病变细胞内有强大的细胞内递送效率和选择性蛋白活性。为了满足这些要求,苏州大学殷黎晨等人开发了一种结合缺氧指导的前蛋白工程和缺氧强化的胞内蛋白递送的级联纳米酶原。
本文要点:
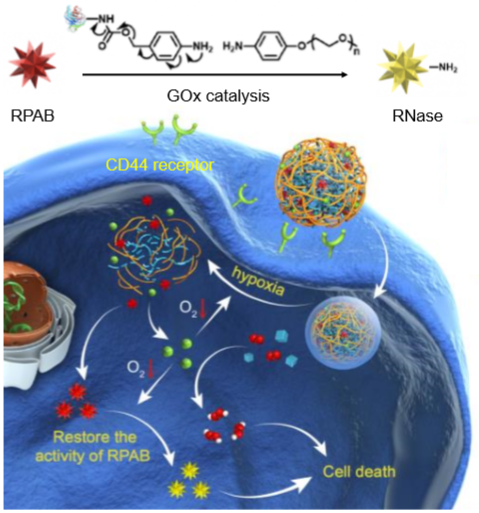
1)RPAB是核糖核酸酶A(RNase A)的前蛋白,在缺氧可裂解的偶氮苯作用下被可逆性封闭,但失去了酶活性。RPAB是利用偶氮苯交联的寡乙烯亚胺(AOEI)和透明质酸(HA)组成的缺氧可解离纳米复合物(NCS)设计而成的,并与葡萄糖氧化酶(GOx)共传递。
2)通过NCS介导的肿瘤靶向、癌细胞内化和内溶酶体逃逸,GOx催化细胞内葡萄糖分解,加剧肿瘤缺氧,促使RPAB恢复到具有水解活性的RNase,同时加速AOEI的降解,释放更多的蛋白质。因此,纳米酶原的催化反应是自加速和自循环的,最终导致GOx介导的饥饿疗法和RNase介导的促凋亡疗法之间的协同抗癌效果。
综上所述,这项研究是首个缺氧指导的前蛋白工程范例,它扩展了可用于蛋白质功能条件控制的化学工具。自催化纳米酶原设计也为介导细胞内蛋白递送和高灵敏度、高选择性的细胞内前蛋白激活提供了一种有效的策略。
Xudong Li, et al. Hypoxia‐instructed pro‐protein therapy assisted with self‐catalyzed nanozymogen. Angew. Chem. Int. Ed., 2020.
DOI: 10.1002/anie.202004008
https://doi.org/10.1002/anie.202004008


















