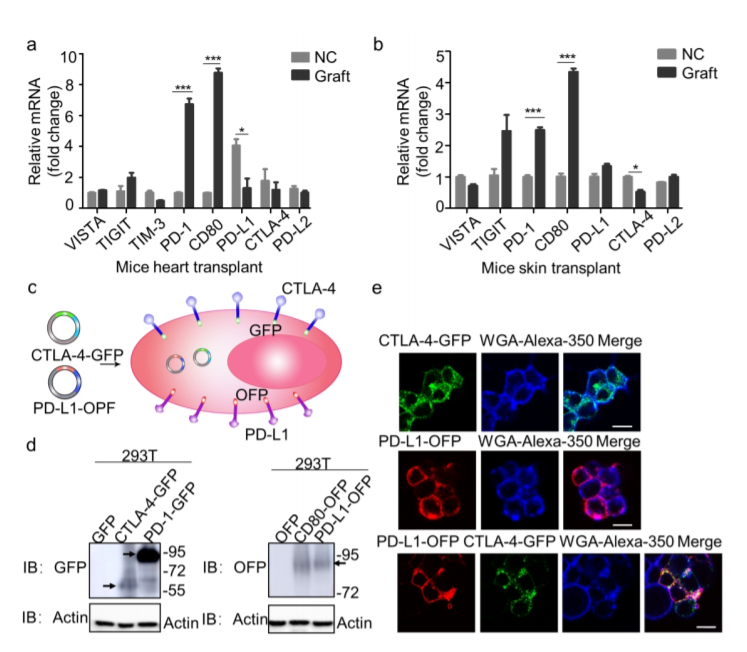
免疫同种异体认知激活T细胞是引发器官排斥的主要因素。器官移植后必须服用免疫抑制药物,但是长期使用这些药物会增加感染和其他严重疾病的风险。于此,中山大学药学院(深圳)陈红波、程芳等人在两个器官移植模型的脾脏中发现程序性细胞死亡配体1/程序性细胞死亡1(PD-L1/PD-1)和细胞毒性T淋巴细胞相关蛋白4/分化簇80(CTLA-4/CD80)的失调。
本文要点:
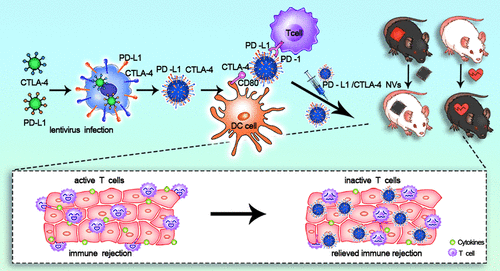
1) 使用生物工程方法,设计了展示PD-L1/CTLA-4双靶货物的细胞外泌体样纳米囊泡(NV),并确定了它们在T细胞和树突状细胞表面结合其配体PD-1和CD80的特异性。因此,这些NV增强了PD-L1/PD-1和CTLA-4/CD80免疫抑制途径,这是共同抑制T细胞活化并维持外周耐受性的两个关键免疫检查点。
2) 还证实了PD-L1/CTLA-4 NVs在体外和体内导致T细胞活化和增殖的减少。最后,证明PD-L1/CTLA-4 NVs降低了CD8+ T细胞的密度和细胞因子的产生,丰富了调节性T细胞,并延长了小鼠皮肤和心脏移植物的存活时间。
综上所述,这些数据支持了PD-L1 / CTLA-4双靶向NV发挥免疫抑制作用,可作为器官移植的一种前瞻性免疫抑制剂。
Zhanxue Xu, et al. Engineering Programmed Death Ligand-1/Cytotoxic T-Lymphocyte-Associated Antigen-4 Dual-Targeting Nanovesicles for Immunosuppressive Therapy in Transplantation. ACS Nano 2020.
DOI: 10.1021/acsnano.9b09065
https://pubs.acs.org/doi/abs/10.1021/acsnano.9b09065


















