肿瘤乏氧、酸性和活性氧过量(ROS)是膀胱肿瘤微环境(TME)的主要特征,TME异常会导致自噬激活,进而促进癌细胞的增殖。与此同时,自噬抑制剂的治疗效果也会受到TME异常的影响。为了解决这些问题,南京大学郭宏骞教授提出了一种新的策略,即利用二氧化锰(MnO2)纳米颗粒对TME进行改善以激活自噬抑制剂,并且改善乏氧和自噬抑制都可使肿瘤细胞对放射治疗更为敏感。
本文要点:
(1)实验利用带负电荷的MnO2和带正电荷的氯喹(CQ)之间的强亲和力,将MnO2和CQ结合在人血清白蛋白(HSA)上制备了纳米颗粒HSA-MnO2-CQ NPs。HSA-MnO2-CQ NPs与H+/H2O2反应后,能在体外有效生成O2,提高pH值,并以对H+/H2O2浓度依赖的方式释放CQ。同时,NPs也可通过增加氯喹的细胞摄取以恢复其在酸性条件下的自噬抑制活性,并显著阻断乏氧诱导的自噬通量。
(2)体内研究表明,该NPs可改善氯喹的药代动力学行为,并在肿瘤组织中有效积累。同时,NPs也可显著减少肿瘤的乏氧区域,提高肿瘤微环境的pH值,对膀胱癌具有显著的自噬抑制作用。综上所述,该HSA-MnO2-CQ NPs可协同调控异常TME和抑制自噬通量,以有效地提高膀胱癌对放疗的敏感性。
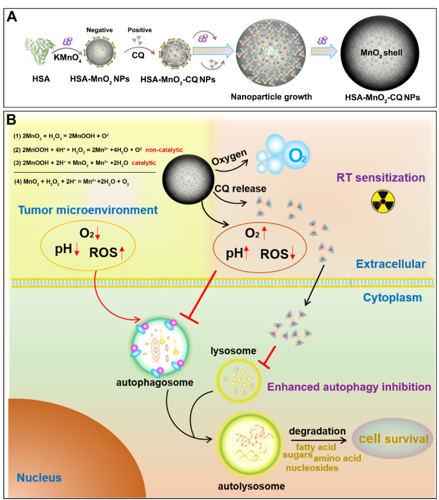
Tingsheng Lin. et al. Synergy of Tumor Microenvironment Remodeling and Autophagy Inhibition to Sensitize Radiation for Bladder Cancer Treatment. Theranostics. 2020
DOI: 10.7150/thno.45358
https://www.thno.org/v10p7683.htm



















