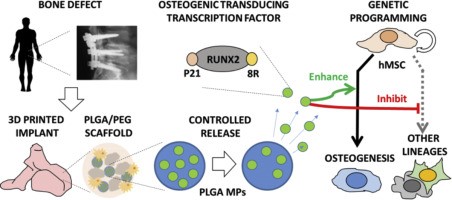
用于制造再生骨组织工程植入物的增材制造工艺不具有生物相容性,因此限制了干细胞的直接使用,并且通常需要在制造后进行细胞接种。在制造过程中结合的机械强度强的生物材料中,干细胞的联合递送与成骨因子的受控释放相结合,将取代可注射的缺损填充物(骨水泥),并使个性化植入物能够通过3D生物打印快速原型化。有鉴于此,英国诺丁汉大学的James E. Dixon等研究人员,通过使用直接遗传程序通过封装在PLGA微粒(MPs)中的外源传递转录因子RUNX2(作为重组GET-RUNX2蛋白传递)的持续释放,证明了人类间充质基质(sMSC)是直接制成可热烧结的3D可生物打印材料,并实现有效的成骨分化。
本文要点
1)重要的是,我们观察到支架中释放的GET-RUNX2(OSX,RUNX2和OPN表达分别增加8.2、3.3和3.9倍)和钙化(von Kossa染色)对基因表达的成骨性编程作用。
2)研发的可生物降解的PLGA / PEG糊剂配方可在缺损模型中增强高密度骨骼的发育(高密度骨骼体积增加约2.4倍),可用于在几分钟内使用温和的细胞相容性快速原型化具有临床尺寸的hMSC植入物挤出生物印刷。
能够创建机械强度高的松质“骨样”可印刷植入物来修复组织的能力,该植入物包含干细胞并控制编程因子的受控释放,这将促进针对许多再生医学应用的直接细胞行为的新型局部递送方法的开发包括用于个性化骨修复的产品。
参考文献:
Hosam Al-Deen M. Abu Awwad, et al. Genetically-programmed, mesenchymal stromal cell-laden & mechanically strong 3D bioprinted scaffolds for bone repair. Journal of Controlled Release, 2020.
DOI:10.1016/j.jconrel.2020.06.035
https://www.sciencedirect.com/science/article/pii/S0168365920303709#f0045


















