肿瘤深部穿透性差和细胞内药物释放不完全目前仍然是抗肿瘤纳米药物临床应用的一大挑战。在此,徐州医科大学附属沭阳医院孙立柱等人开发了一种纳米药物--RLPA-NPs,可实现延长血液循环、肿瘤深部渗透、主动靶向癌细胞、内体/溶酶体逃逸和细胞内选择性自增强药物释放的功能,从而实现有效的药物递送。
本文要点:
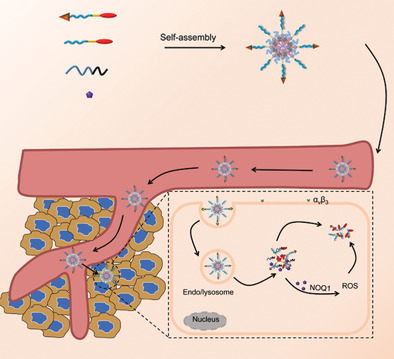
1)RLPA-NPs由pH敏感的聚合物十八胺聚(天冬氨酸-1-氨基丙基)咪唑(OA-P(Asp-API))和活性氧生成剂β-拉帕酮(Lap)包裹在由肿瘤穿透肽内化RGD(iRGD)修饰的活性氧反应性紫杉醇(PTX)前药组装的胶束中构建而成。
2)iRGD可促进RLPA-NPs深入肿瘤组织,并特异性靶向肿瘤细胞。OA-P(Asp-API)通过受体介导的内吞作用被癌细胞内化后,可在内体的酸性环境中迅速质子化,导致RLPA-NPs通过“质子海绵效应”逃逸内体。同时,RLPA-NPs胶束解体,释放出Lap和PTX前药。随后,释放的Lap可以产生ROS,从而放大并加速PTX的释放,进而杀伤肿瘤细胞。
3)体内和体外研究表明,与对照组相比,RLPA-NPs能显著提高治疗效果。
综上所述,RLPA-NPs是一种很有前景的纳米平台,可以克服多种生理和病理障碍,增强药物递送。
Yongfei Li, et al. Dual pH/ROS‐Responsive Nanoplatform with Deep Tumor Penetration and Self‐Amplified Drug Release for Enhancing Tumor Chemotherapeutic Efficacy. Small, 2020.
DOI: 10.1002/smll.202002188
https://doi.org/10.1002/smll.202002188


















