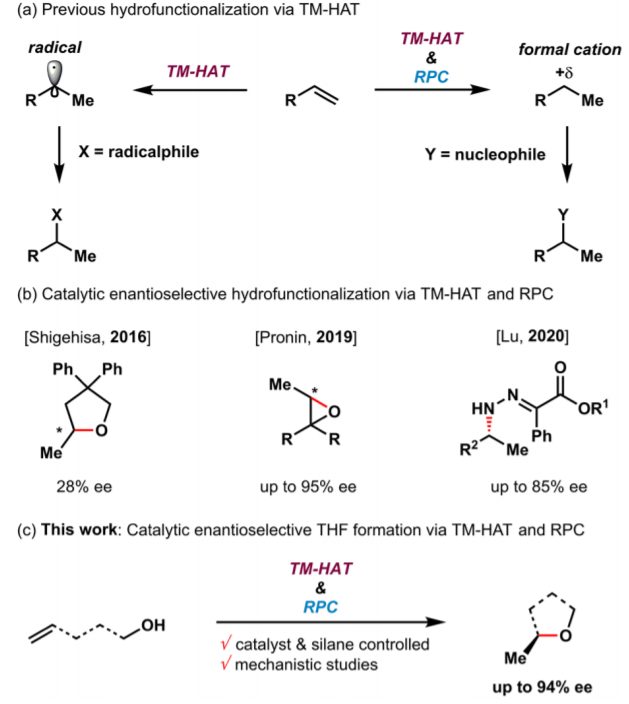
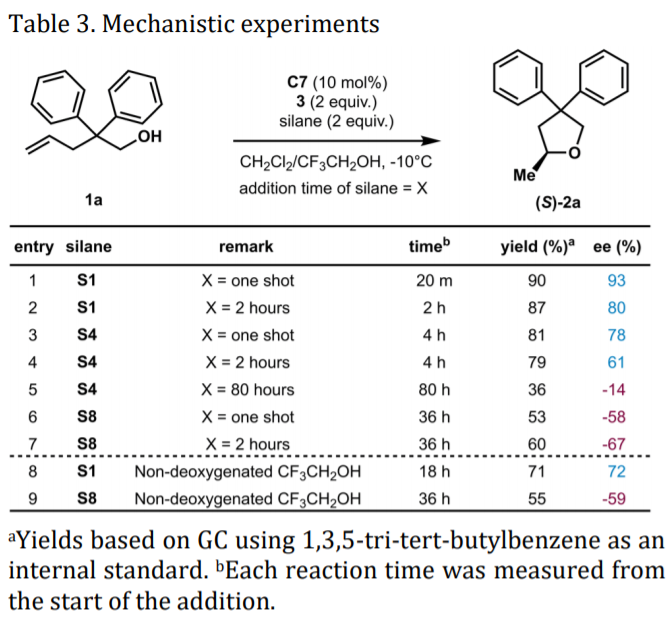
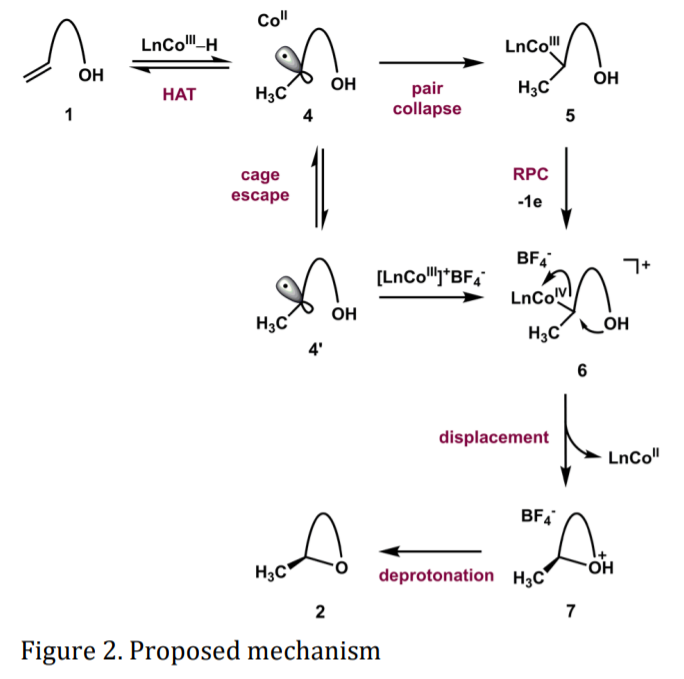
武藏野大学Hiroki Shigehisa等报道催化不对称合成四氢呋喃衍生物类产物,这种结构在天然产物分子中广泛存在,该方法具体通过过渡金属催化的氢原子转移反应(HAT,hydrogen atom transfer)和自由基极性翻转过程进行,通过一种手性钴催化剂实现了最高达到94 % ee值的反应。特别有意思的是,产物的绝对构型和硅烷分子的立体位阻结构有非常大的相关性。作者通过缓慢加入硅烷,溶剂,热化学过程,DFT模拟等方法验证了反应在两种竞争性反应的过程中的选择性。当反应中使用立体位阻效应较低的二乙基硅烷,当较高浓度的碳中心自由基物种引发了烷基钴(III)中间体的自由基链反应并产生对映体富集,并决定了产物的绝对构型。与之相比,当硅烷的立体位阻效应较高时,自由基链反应的发生会受到抑制,因此会在烷基钴(IV)中间体的后期亲核取代反应中有效的进行对映选择性的动力学拆分反应。
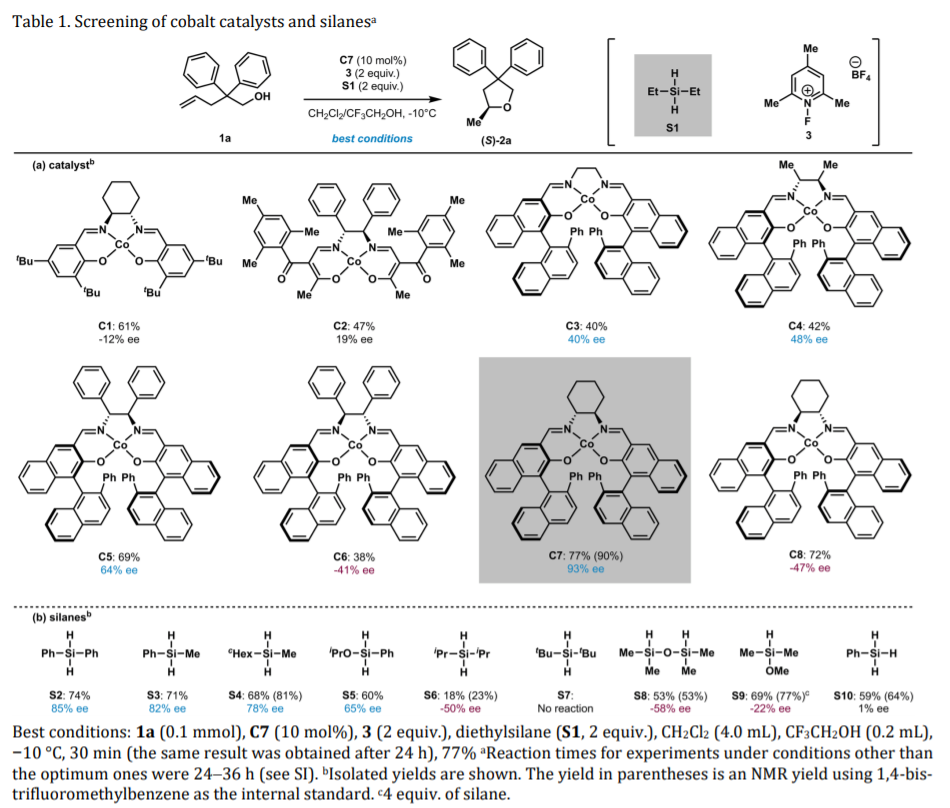
反应优化。将二苯基修饰的烯戊醇(1a)作为反应物,加入2倍量三甲基吡啶氟硼氟酸盐(3),2倍量二乙基硅氢(S1),10 mol %手性Co催化剂,在-10 ℃的CH2Cl2/CF3CH2OH混合溶剂中进行反应。对手性钴催化剂的手性配体结构进行调控,结果显示双亚胺双酚配位的Co催化剂中当双亚胺桥上修饰环己烷有最好的手性选择性。在优化的反应条件中实现了93 % ee选择性和77 %产率。对硅烷分子的结构进行筛选,结果发现双苯基硅烷,该反应的手性选择性降低为85 % ee,产率稍有降低(74 %);对苯基甲基硅烷作为反应物,该反应的手性选择性降低为82 % ee,产率降低为71 %;当苯硅烷作为反应物,该反应的手性选择性降低为1 % ee,产率降低为59 %;当双叔丁基硅烷作为反应物,该反应无法进行;当双异丙基硅烷作为反应物,反应的手性选择性发生翻转,同时手性选择性降低为-50 % ee。
参考文献
Kousuke Ebisawa, Kana Izumi, Yuka Ooka, Hiroaki Kato, Sayori Kanazawa, Sayura Komatsu, Eriko Nishi, and Hiroki Shigehisa*
Catalyst- and Silane-Controlled Enantioselective Hydrofunctionalization of Alkenes by Cobalt-Catalyzed Hydrogen Atom Transfer and Radical-Polar Crossover, J. Am. Chem. Soc. 2020
DOI:10.1021/jacs.0c05017
https://pubs.acs.org/doi/10.1021/jacs.0c05017


















