由于实体肿瘤内的微环境具有乏氧的特点,因此光动力治疗(PDT)的抗癌效果往往很有限。大连理工大学孙文副研究员、樊江莉教授和马克斯·普朗克聚合物研究所Katharina Landfester构建了一种由卵白蛋白包封的纳米胶囊以介导进行协同PDT-化学治疗,该策略可通过增强活性氧(ROS)的生成以显著改善抗癌治疗效果。
本文要点:
(1)可被生物降解的蛋白纳米胶囊可以高效地包封多种功能试剂,包括S取代的光敏剂尼罗蓝(NBS)、顺铂药物和用于芬顿反应的Fe3O4纳米颗粒。研究表明 ,即使在严重的乏氧环境(2% O2)下,光敏剂NBS也可以表现出优越的I型PDT疗效。
(2)PDT产生的O2•−可在超氧化物歧化酶(SOD)的作用下转化为H2O2。随后,共载的Fe3O4纳米颗粒可提供Fe2+以通过类芬顿反应将H2O2转化为高毒性的•OH。PDT也会进一步促进活性物质的核内体/溶酶体逃逸,从而增强它们在细胞内的转运,并且在耐药细胞中也是如此。与此同时,当有烟酰胺腺嘌呤二核苷酸磷酸氧化酶(NOX)存在时,顺铂也会生成O2•−以提高•OH的产量,进而增强治疗效果。
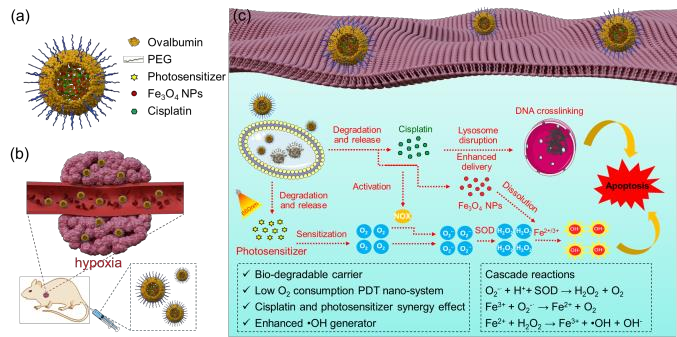
Shuai Jiang. et al. Synergistic Anticancer Therapy by Ovalbumin EncapsulationEnabled Tandem ROS Generation. Angewandte Chemie International Edition. 2020
DOI: 10.1002/anie.202006649
https://onlinelibrary.wiley.com/doi/10.1002/anie.202006649



















