在光动力疗法(PDT)中,活性氧(ROS)触发的自噬通常表现出抗凋亡作用,促进细胞存活。在此,浙江大学金桥等人构建了一种创新的超分子纳米平台,通过将自噬的作用从促生存转变为促死亡来增强PDT。
本文要点:
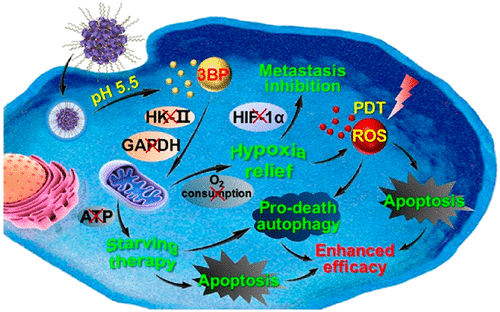
1)呼吸抑制剂3-溴丙酮酸(3BP)可作为自噬启动剂和缺氧改善剂,将其集成到光敏剂chlorin e6(Ce6)封装的纳米颗粒中对抗缺氧肿瘤。3BP通过下调HK-II和GAPDH表达抑制呼吸,显著降低细胞内耗氧率,缓解肿瘤缺氧,促进光动力肿瘤治疗。
2)更重要的是,通过Western blot、免疫荧光成像和透射电镜观察,3BP和PDT联合应用,自噬水平显著升高。
3)令人惊讶的是,过度激活的自噬促进了细胞凋亡,导致自噬由促生存转变为促死亡。因此,PDT联合3BP可以有效抑制细胞增殖,消除肿瘤。
4)肿瘤缺氧被3BP缓解后,缺氧诱导因子-1α(HIF-1α)可下调。通过消除原发肿瘤和下调HIF-1的表达,可以有效抑制肿瘤转移。
这些结果为未来通过触发死亡自噬来治疗癌症的创新方法提供了启发。
Yongyan Deng, et al. 3-Bromopyruvate-Conjugated Nanoplatform-Induced Pro-Death Autophagy for Enhanced Photodynamic Therapy against Hypoxic Tumor, ACS Nano, 2020.
DOI: 10.1021/acsnano.0c01350
https://doi.org/10.1021/acsnano.0c01350


















