靶向患者特异性新抗原的癌症疫苗已成为改善免疫检查点阻断反应的一种有前途的策略。然而,新的抗原肽免疫原性差,不能刺激CD8+T细胞应答,因此需要新的疫苗技术来增强其免疫原性。干扰素基因刺激因子(STING)途径是一种内源性机制,通过该机制,先天性免疫系统产生一个免疫环境来启动和动员新抗原特异性T细胞。在此,美国范德比尔特大学John T. Wilson等人开发了一种模拟免疫原性癌细胞的合成癌症纳米疫苗平台(nanoSTING-vax),它能有效地促进肽抗原和刺激剂cGAMP的共递送。
本文要点:
1)将cGAMP和多肽共负载到pH响应性的内溶性多聚体中,促进cGAMP和肽抗原协同递送到胞浆,从而诱导炎性细胞因子的产生,共刺激标志物的表达,以及抗原的交叉呈递。因此,nanoSTING-vax显著增强了CD8+T细胞对一系列肽抗原的反应。
2)nanoSTING-vax治疗性免疫联合免疫检查点阻断可抑制多种肿瘤模型的肿瘤生长,甚至导致肿瘤完全排斥反应和持久的抗肿瘤免疫记忆的产生。
总而言之,这项工作建立了nanoSTING-vax作为一个多功能平台,用于增强对新抗原靶向癌症疫苗的免疫反应。
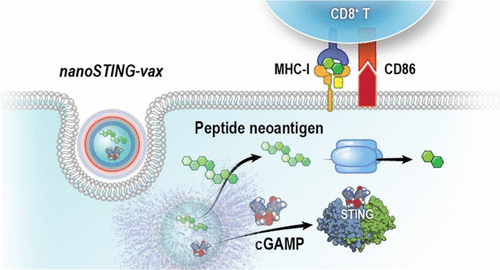
Daniel Shae, et al. Co-delivery of Peptide Neoantigens and Stimulator of Interferon Genes Agonists Enhances Response to Cancer Vaccines, ACS Nano, 2020.
DOI: 10.1021/acsnano.0c02765
https://doi.org/10.1021/acsnano.0c02765


















