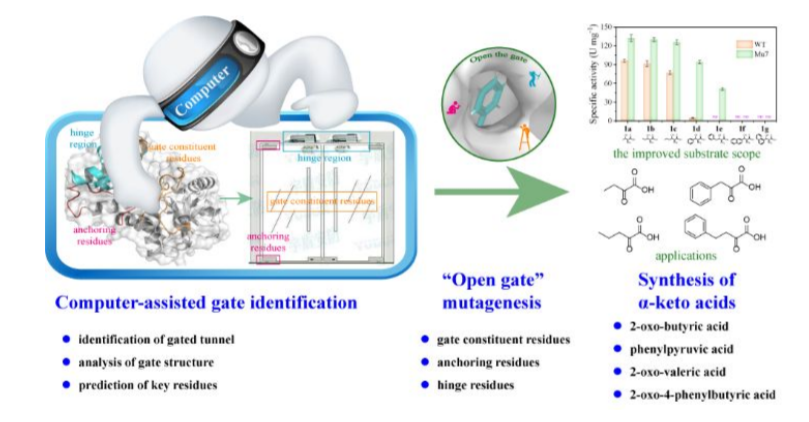
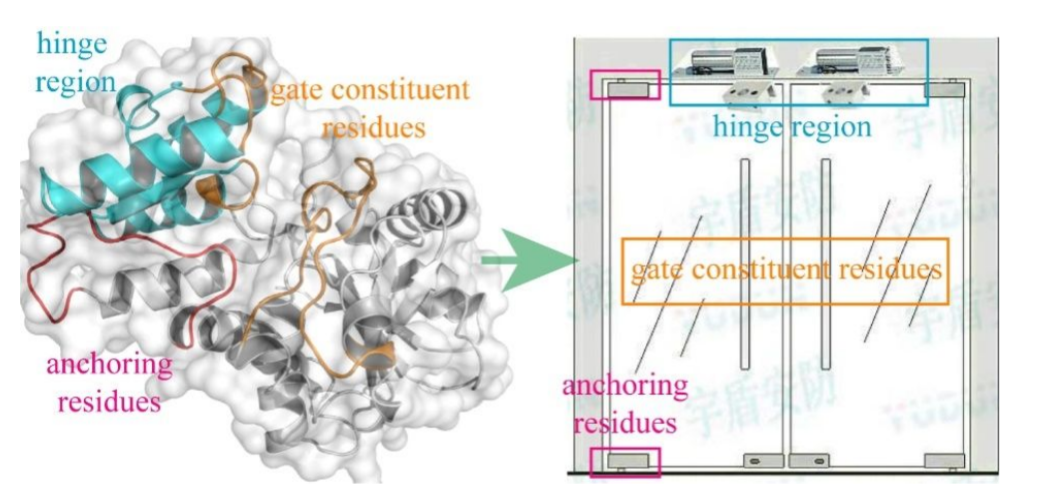
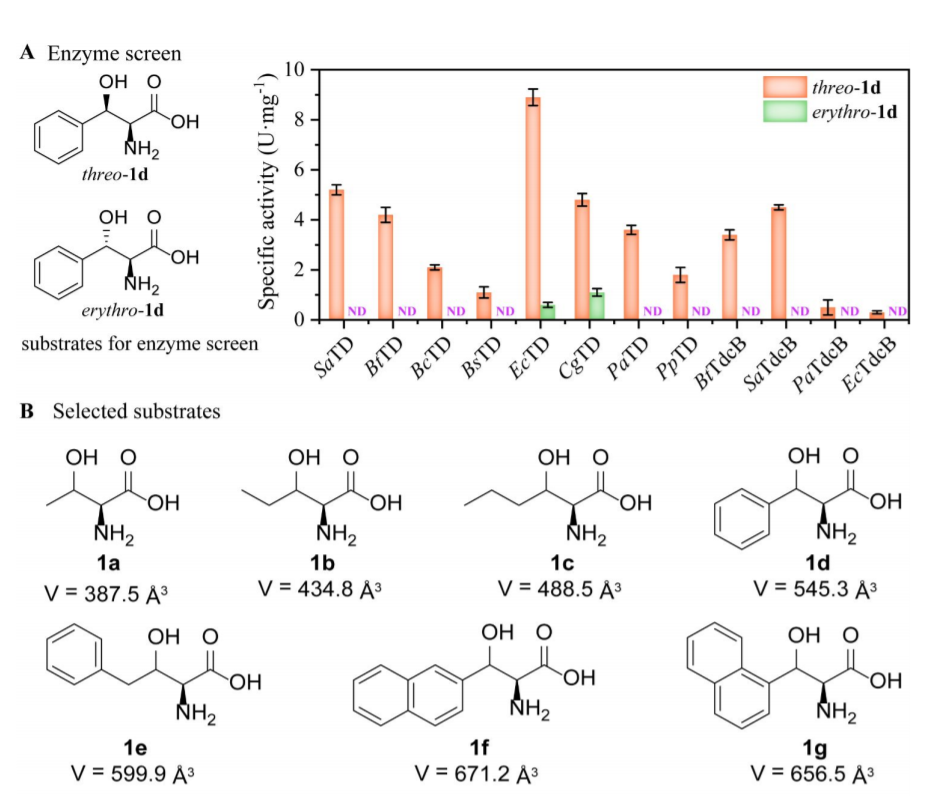
苏氨酸脱氨酶Threonine deaminase(EC 4.3.1.19)催化的α,β-消除(脱胺基)反应在合成非天然α-酮酸中具有一定潜力,但是天然苏氨酸脱氨酶种类较少,导致其应用范围受到一定限制。有鉴于此,江南大学刘立明等报道了谷氨酸棒杆菌型苏氨酸脱氨酶CgTD(Corynebacterium glutamicum)作为模型,发现通过底物通道起到门控作用,实现了合成非天然α-酮酸。
基于这种门控作用机制和底物通道作用,实现了一种“开门”策略改善了底物的种类。其中优化后得到的CgTDMu7展现了催化性能实现了90.6倍的提高(例如苯丝氨酸的催化反应),作者发现这种改善的催化反应活性是通过更高效率的底物耦合、脱氢反应、亚胺水解反应实现的。作者发现CgTDMu7能够有效的制备天然和非天然α-酮酸分子,包括2-氧代丁酸(83.4 g L-1,转化率99 %),苯丙酮酸(72.5 g L-1,转化率95 %),2-氧代戊酸(21.1 g L-1,转化率91 %),2-氧代-4-苯基丁酸(29.9 g L-1,转化率84 %)。
参考文献
Wei Song, Xin Xu, Cong Gao, Yuxuan Zhang, Jing Wu, Jia Liu, Xiulai Chen, Qiuling Luo, and Liming Liu*
Open the Gate of Corynebacterium glutamicum Threonine Deaminase for Efficient Synthesis of Bulky α-Keto Acids, ACS Catal. 2020
DOI:10.1021/acscatal.0c01672
https://pubs.acs.org/doi/10.1021/acscatal.0c01672


















