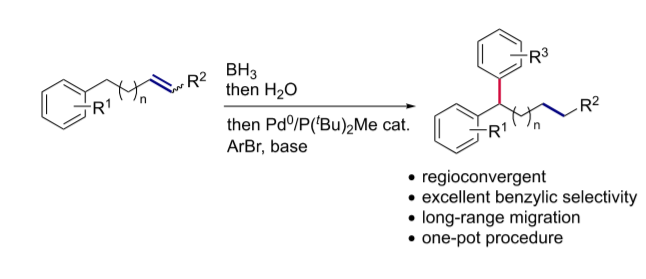
链行走反应是一种远程实现C-H键官能团化的方法,尽管过去一段时间内多种Pd催化交叉移动反应被发展,但是仍然没有一种实现Suzuki-Miyaura交叉偶联反应的有效方法,有鉴于此,巴塞尔大学Olivier Baudoin等报道了一种一锅合成方法,通过烯烃进行氢硼化反应类似的机理进行反应,发现在P(tBu)2Me配体配合中进行邻位芳基亲电反应。同时展示了烯烃位置和几何异构体的区域收敛、长程移动情况。作者对该反应中的可逆的、非切断反应机理进行研究。
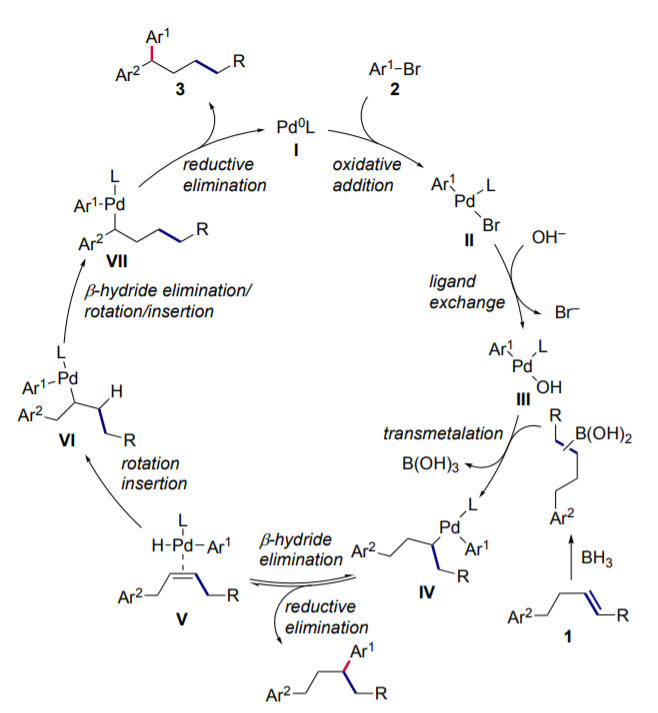
反应机理。Pd0L对芳基溴化物氧化加成生成Pd中间体(II),随后和OH-进行配体和Br-交换反应,生成Pd(OH)中间体III。同时BH3对芳基修饰烯烃底物(1)上的烯烃进行活化,随后对Pd中间体III进行转金属化反应,消除B(OH)3的同时,得到烷基Pd中间体物种IV。通过β-氢化物消除过程形成Pd-烯烃配合物中间体V,通过接连多步Pd-H插入/β-氢化物消除连续反应过程,得到Pd加成到苄基位点的中间体物种VII,最后通过还原消除过程得到1,1-双芳基修饰烷烃产物。
参考文献
Yann Baumgartner and Olivier Baudoin*
One-Pot Alkene Hydroboration/Palladium-Catalyzed Migratory Suzuki-Miyaura Cross-Coupling, ACS Catal. 2020
DOI: 10.1021/acscatal.0c02755
https://pubs.acs.org/doi/10.1021/acscatal.0c02755


















