尽管三阴性乳腺癌(TNBC)对靶向激素治疗有耐药性,但偶氮苯康普瑞汀A4(Azo-CA4)的发现为TNBC提供了治疗机会。在此,天津大学Yanjun Zhao、Zheng Wang等人将Azo-CA4负载在可以将近红外光转换为紫外光以激活Azo-CA4的上转换纳米载体中,显著降低了TNBC细胞的存活率。
本文要点:
1)辐照后,负载Azo-CA4的纳米载体通过凋亡和铁下垂显著降低TNBC细胞的存活率。前者是由Azo-CA4的光异构化诱导的,并伴有微管破裂和细胞周期阻滞于G2/M期。后者是由于紫外光诱导Fe3+还原为Fe2+,以促进脂质的过氧化。
2)在异种移植小鼠模型中,从组织学染色、肿瘤生长抑制和动物存活等方面证实了细胞凋亡和铁下垂在消除TNBC方面表现出的协同作用。由于近红外光仅适用于肿瘤部位,这种触发的纳米载体对健康器官的不良影响可以忽略不计。
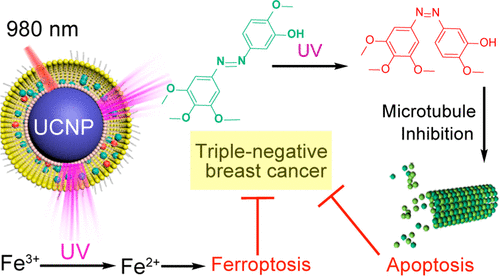
Jundong Zhu, et al. Upconverting Nanocarriers Enable Triggered Microtubule Inhibition and Concurrent Ferroptosis Induction for Selective Treatment of Triple-Negative Breast Cancer. Nano Lett., 2020.
DOI: 10.1021/acs.nanolett.0c00502
https://doi.org/10.1021/acs.nanolett.0c00502


















