肝脏是乳腺癌最常见的转移部位之一,具有很高的致死率。虽然肿瘤细胞与其转移部位的微环境之间的相互作用已被认为是肿瘤进展的关键调节因素,但其潜在的机制尚未完全阐明。在此,韩国蔚山国立科学技术学院Yoon-Kyoung Cho等人描述了一种三维(3D)微流控人类肝芯片(肝芯片),它模拟了转移前生态位的形成,以研究乳腺癌源性细胞外小泡(EVs)在肝转移中的作用。
本文要点:
1)实验证明乳腺癌源性EVs激活了肝芯片中的肝窦内皮细胞(LSECs),诱导内皮细胞向间充质的转化和血管屏障的破坏。
2)研究还发现乳腺癌源性EVs中的转化生长因子β1(TGFβ1)上调了LSECs上的纤维连接蛋白(一种黏附的细胞外基质蛋白),从而促进了乳腺癌细胞与肝脏微环境的粘附。
3)此外,研究发现与健康供者或非转移性TNBC患者分离的EVS相比,三阴性乳腺癌(TNBC)肝转移患者的EVs含有更高的TGFβ1水平,并诱导更多的乳腺癌细胞粘附到3D人肝芯片上。
综上所述,这些发现为更好地理解乳腺癌源性EVs引导肝脏继发转移的机制提供了更好的理解。此外,这项研究中描述的3D人肝芯片为研究肝脏继发性转移的潜在机制和可能的治疗策略提供了一个平台。
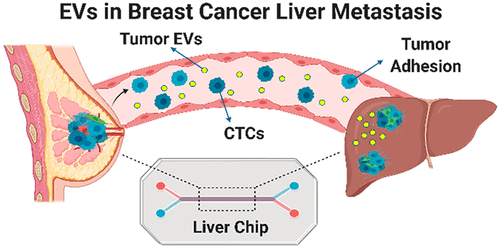
Junyoung Kim, et al. Three-Dimensional Human Liver-Chip Emulating Premetastatic Niche Formation by Breast Cancer-Derived Extracellular Vesicles. ACS Nano, 2020.
DOI: 10.1021/acsnano.0c04778
https://doi.org/10.1021/acsnano.0c04778


















