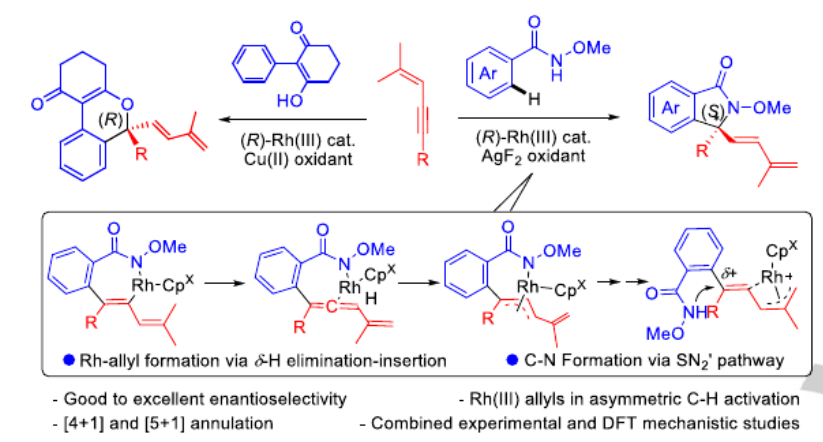
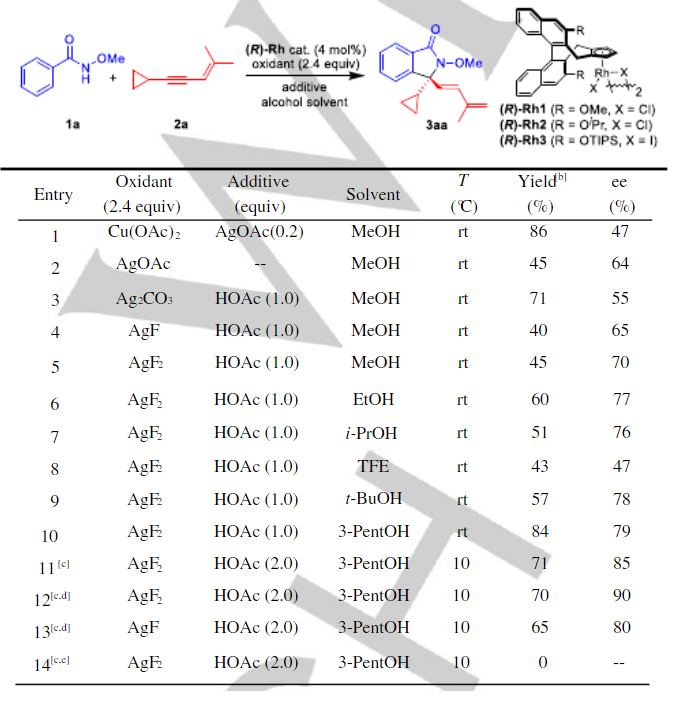
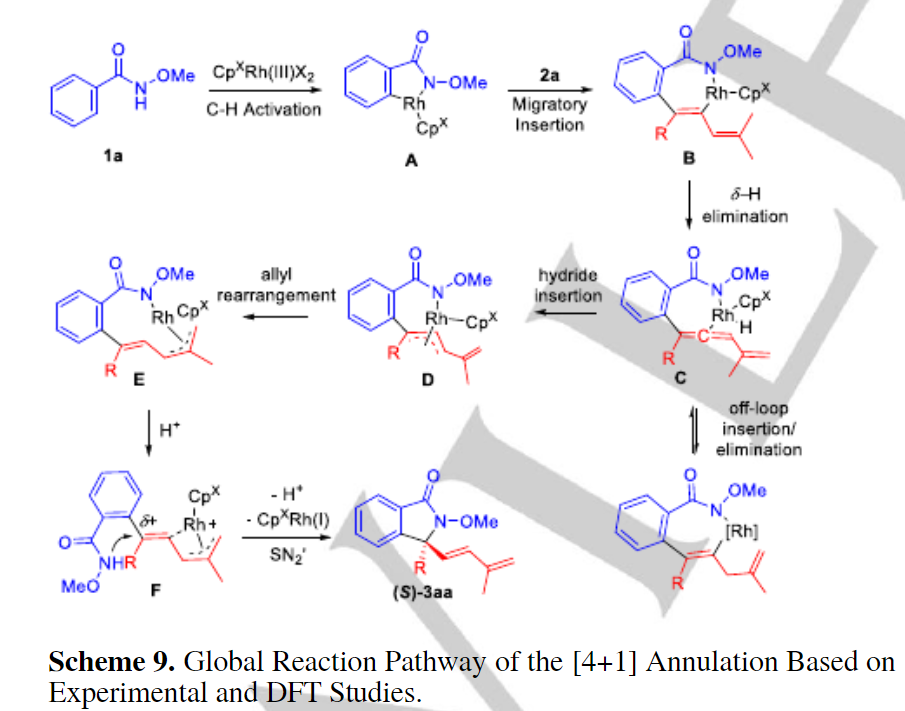
金属烯丙基在多种偶联反应中起到作用,具有较高的反应活性,但是Rh(III)π-烯丙基物种鲜有用于不对称C-H键官能团化反应中。有鉴于此,大连化学物理研究所李兴伟等报道了芳烃、1,3-烯炔作为反应物,通过手性环戊二烯基Rh(III)经由氧化性[4+1]、[5+1]成环进行对映选择性催化合成内酰胺、异苯并吡喃等产物。该反应通过C-H键活化、烯基向烯丙基的重排、亲核环化级联实现。
参考文献
Jiaqiong Sun, Weiliang Yuan, Rong Tian, Peiyuan Wang, Xue-Peng Zhang, Xingwei Li*
Rhodium(III)‐Catalyzed Asymmetric [4+1] and [5+1] Annulation of Arenes and 1,3‐Enynes: Distinct Mechanism of Allyl Formation and Allyl Functionalization, Angew. Chem. Int. Ed. 2020
DOI: 10.1002/anie.202010832
https://www.onlinelibrary.wiley.com/doi/10.1002/anie.202010832