高端的仿生设计一直是广大科研工作者所追求的目标,这些仿生材料在许多领域显示出了巨大的优势。在细胞中,物质运输对于复杂的生命活动必不可少,主要包括浓度梯度引起的细胞膜被动传递和刺激传递。合理设计制备一种能够实现连续质量释放的人工细胞是当前仿生科学领域一个重要的方向。中空多壳层结构(HoMSs)与细胞结构相似,在壳体内具有相对独立的空腔和孔道。有鉴于此,中国科学院过程工程研究所的Dan Wang和Suojiang Zhang等受细胞中不同的物质运输模式的启发,系统研究了中空多壳层结构中的质量运输过程。
本文要点:
1)将抗菌剂甲基异噻唑啉酮(MIT)作为模型分子引入到HoMSs中,发现了一个三步连续的释放阶段,即突释、缓释和刺激反应性释放。
2)在相同条件下,三层壳层结构的抗菌效果是纯抗菌剂的8倍左右。
3)HoMS系统拥有环境变化触发的智能响应释放机制。
4)由化学扩散和物理阻碍共同驱动的时空有序药物释放过程为智能纳米材料的设计提供了一条新的途径。
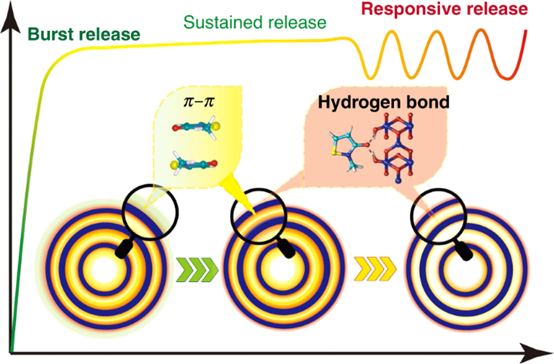
Zhao, D., Yang, N., Wei, Y. et al. Sequential drug release via chemical diffusion and physical barriers enabled by hollow multishelled structures. Nat Commun 11, 4450 (2020).
DOI: 10.1038/s41467-020-18177-2
https://doi.org/10.1038/s41467-020-18177-2



















