目前,抗肿瘤免疫治疗的临床应用仍面临着与疗效相关的严峻挑战。在此,武汉大学张先正等人设计了一种光触发核壳纳米系统,旨在通过控制释放抗PD-L1(αPD-L1)抗体和增强抗原提呈来增强抗肿瘤免疫反应。
本文要点:
1)以金纳米棒(Au NRs)为光热核,沸石咪唑框架-8(ZIF-8)为壳用于αPD-L1递送,并进一步聚乙二醇化构建了纳米系统--AZ-P@P。
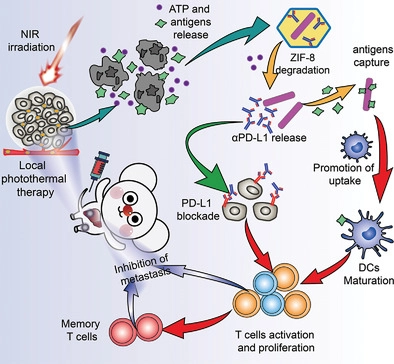
2)在此纳米系统中,ZIF-8外壳保护αPD-L1抗体免受复杂的生理环境和高温的影响。一旦在肿瘤部位聚集,AZ-P@P在近红外线(NIR)光触发加热下诱导肿瘤细胞死亡,释放肿瘤衍生蛋白抗原(TDPAs)和三磷酸腺苷(ATP)。此后,释放的ATP降解ZIF-8外壳,暴露出Au NRs,通过捕获TDPA并将其转运到树突状细胞(DC)来促进T细胞在肿瘤内的浸润。同时,大量的αPD-L1在原位释放,以恢复T细胞活性。
3)机制研究表明,AZ-P@P可促进DC的成熟和活化T细胞的浸润,从而诱导强大的抗肿瘤免疫。研究表明,近红外光触发的AZ-P@P能显着破坏原发肿瘤,抑制转移。
综上所述,这种多重免疫调节系统为肿瘤治疗提供了一种很有前途的工具。
Qian Cheng, et al. Near‐Infrared Triggered Cascade of Antitumor Immune Responses Based on the Integrated Core–Shell Nanoparticle. Adv. Funct. Mater., 2020.
DOI: 10.1002/adfm.202000335
https://doi.org/10.1002/adfm.202000335


















