实体瘤的乏氧微环境严重限制了光动力治疗(PDT)的效果。因此,开发可以共负载光敏剂和氧气、并具有成像性能的纳米载体对于癌症诊疗来说具有重要意义。复旦大学施裕新教授、上海交通大学Han Wang和同济大学张兵波教授利用基于人内源性蛋白血红蛋白(Hb)的仿生合成策略构建了一种Gd基纳米结构,并将其用于同时负载Ce6和氧气,缓解肿瘤乏氧环境,实现磁共振成像(MRI)指导的增强PDT。
本文要点:
(1)Gd@HbCe6-PEG纳米结构是通过绿色和蛋白仿生方法合成的。实验在体内外对Gd@HbCe6-PEG的理化性质,包括弛豫性质、携氧/释放氧能力和PDT疗效等。实验结果表明,Gd@HbCe6-PEG纳米结构具有多样性的功能,可以通过MRI对肿瘤进行成像以及指导PDT。光谱分析和体外氧检测器则证明了Gd@HbCe6-PEG具有良好的携氧能力。
(2)此外,实验也通过光声成像和免疫荧光染色验证了静脉注射Gd@HbCe6-PEG后其在体内缓解肿瘤乏氧的作用,并通过形态学和功能磁共振成像观察了早期PDT的治疗效果。与此同时,Gd@HbCe6-PEG可在治疗后通过肾脏被快速清除。因此,这一研究也为利用基于人内源性蛋白的仿生合成策略开发可同时进行肿瘤氧化和成像指导的增强PDT的多功能纳米探针提供了新的思路。
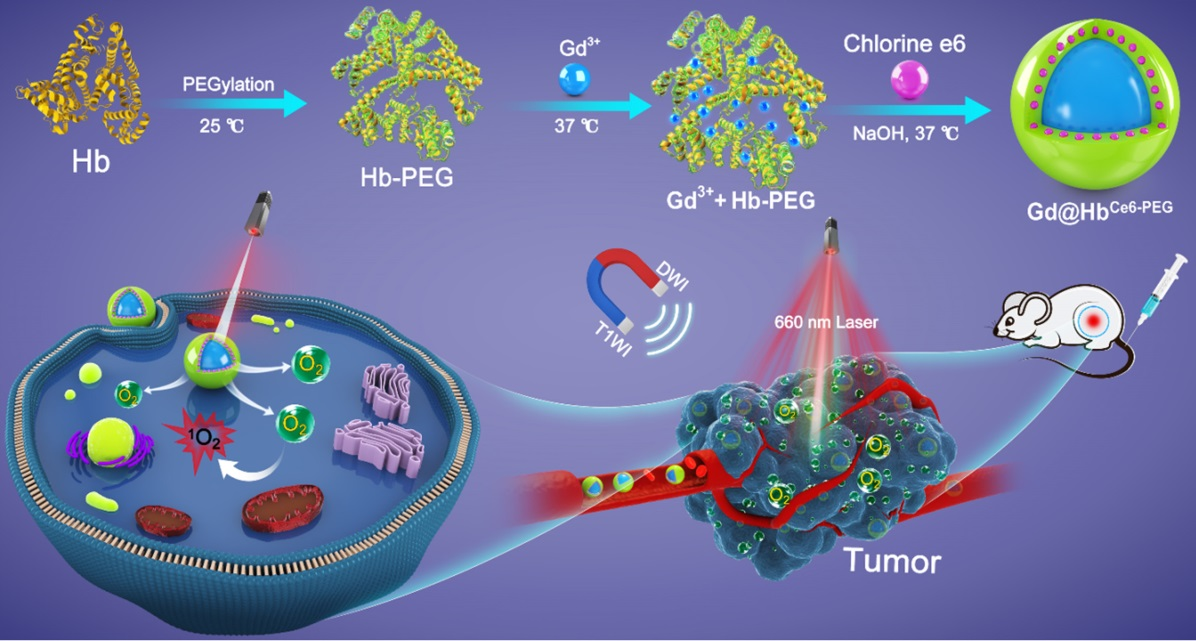
Xiudong Shi. et al. Hemoglobin-mediated biomimetic synthesis of paramagnetic O2-evolving theranostic nanoprobes for MR imaging-guided enhanced photodynamic therapy of tumor. Theranostics. 2020
DOI: 10.7150/thno.46228
https://www.thno.org/v10p11607.htm



















